Định lượng IL-2R (hay CD25 hòa tan) trong huyết thanh bằng kỹ thuật miên dịch gắn men (Elisa) - Bộ y tế 2017
I. NGUYÊN LÝ
Kháng thể (KT) kháng IL-2R người được hấp ph vào giếng x t nghiêm. Khi thêm huyết thanh người bệnh vào giếng x t nghiệm, IL-2R trong huyết thanh người bệnh được gắn đặc hiệu lên các KT này trong giếng, tạo nên phức hợp KN - KT. Kháng thể kháng IL-2R người kết hợp với HRP (có enzyme peroxidase) được thêm vào ở bước tiếp theo sẽ gắn tiếp t c lên IL-2R trong mẫu huyết thanh. Sau khi ủ và rửa, các kháng thể thừa được loại b . Dung dịch cơ chất được thêm vào giếng, phản ứng với HRP tạo màu. Sản phẩm màu được tạo ra tương ứng với lượng IL-2 có mặt trong mẫu huyết thanh. Phản ứng kết thúc khi thêm dung dịch dừng phản ứng (có chứa acid). Đo m t độ quang (OD) ở bước sóng 450 nm. Một đường cong chuẩn được h nh thành từ 7 mẫu IL-2R chuẩn (đã biết n ng độ) được pha loãng. Đường chuẩn này được thiết l p với mỗi phiến x t nghiệm. N ng độ IL-2R của mẫu huyết thanh được xác định d a trên đường chuẩn này.
II. CHỈ ĐỊNH
Các trường hợp có s gia tăng hoạt tính của tế bào lympho T: Hội chứng th c bào tế bào máu, Lơ xê mi tế bào tóc, U lympho Hodgkin, không Hodgkin; các bệnh t miễn hoặc nhiễm khuẩn như bệnh Kawasaki, Xơ cứng bi rải rác, bệnh Lupus ban đ hệ thống; bệnh lý thải ghép,...
III. CHỐNG CHỈ ĐịNH
Không có chống chỉ định.
IV. CHUẨN BỊ
1. Người thực hiện
- Kỹ thuật viên và cử nhân đã được đào tạo thực hiện kỹ thuật;
- Bác sĩ xét nghiệm: đọc kết quả, đánh giá, kiểm tra chất lượng.
2. Phương tiện - Hóa chất
2.1. Phương tiện
- Máy ly tâm ống máu;
- Pipet và đầu pipet loại 25μl và 1000μl;
- Dàn máy ELIS (t động hoặc bán t động);
- Găng tay.
2.2. Hóa chất
Kít định lượng IL-2R g m các thành phần sau:
- Phiến x t nghiệm 96 giếng có phủ KT đơn d ng kháng IL-2R người (Coated Microwell Strips): phiến được đ ng trong túi bạc.
- Dung dịch cộng hợp- Kháng thể đơn d ng kháng IL-2R người kết hợp HRP (HRP conjugate): lọ 70ul, nắp vàng.
- IL-2R người đông khô, sau tái h a tan đạt n ng độ 40ng/ml (sIL-2R Standard): 2 lọ 250ul, nắp màu xanh.
- Dung dịch pha loãng mẫu (Sample Diluent): lọ 12ml, nắp màu đen.
- Dung dịch đệm 20x, chứa dung dịch PBS 1% -20% và 10% BS ( ssay Buffer Concentrate 20x): lọ 5ml, nắp trắng.
- Dung dịch đệm rửa 20x, chứa PBS 1%-20% (Wash buffer concentrate 20x): lọ 50ml, nắp đen.
- Dung dịch cơ chất tetramethyl-benzidin (Substrate Solution): lọ 15ml, nắp xanh.
- Dung dịch dừng phản ứng, chứa dung dịch acid phosphoric 1M (Stop solution): lọ 15ml, nắp vàng.
- Miếng dán ( dhesive Films): g m 2 miếng dán được đóng gói trong bao nilon; Hóa chất khác: Nước cất, hoá chất khử trùng Natri hypoclorite.
3. Mẫu bệnh phẩm
- Mẫu dùng là huyết thanh.
- Cần tách huyết thanh càng sớm càng tốt để tránh hiện tượng tan máu làm ảnh hưởng đến kết quả phản ứng.
- Nếu có lẫn h ng cầu hoặc những thành phần hữu hình trong mẫu huyết thanh thì cần ly tâm mẫu để loại b các thành phần đó trước khi xét nghiệm.
- Mẫu huyết thanh bảo quản ở nhiệt độ 2oC đến 8oC có thể dùng làm xét nghiệm trong vòng 7 ngày. Nếu muốn để l u hơn mới x t nghiệm cần phải bảo quản ở tủ lạnh sâu (≤ -20oC). Tuy nhiên với mẫu bảo quản lạnh s u cần tránh đông-tan nhiều lần.
V. CÁC BƯỚC TIẾN HÀNH
- Chuẩn bị giếng: rửa phiến 2 lần với 400ul dung dịch đệm rửa, cách nhau 10-15 gi y.
- Pha dung dịch pha loãng 20X (sample buffer) thành dung dịch 1X. VD 20ml dung dịch 1X (1ml dung dịch 20X + 19ml nước cất H2O).
- Pha IL-2R người đông khô về đúng n ng độ 40ng/ml.
- Nh 100ul dung dịch pha loãng mẫu vào các giếng chuẩn. Nh 50ul dung dịch pha loãng mẫu vào giếng x t nghiệm.Nh 50ul huyết thanh vào giếng x t nghiệm.
- Thêm 50ul dung dịch cộng hợp.
- Ủ 30 phút ở nhiệt độ ph ng.
- Rửa 3 lần bằng dung dịch rửa, 400μl /giếng/lần.
- Nh 100μl cơ chất tạo mầu (TMB subtrate) vào mỗi giếng.
- Ủ 30 phút ở nhiệt độ ph ng, tránh ánh sáng.
- Nh 100μl dung dịch dừng phản ứng (stop solution) vào mỗi giếng theo đúng tr nh t nh TMB.
- Đọc phiến ở bước sóng 450/620 nm (tốt hơn th dùng bước sóng k p 450/ 620 nm) trong v ng 30 phút sau khi ủ dung dịch ngừng phản ứng.
- Phân tích kết quả.
VI. NHẬN ĐỊNH KẾT QUẢ
- Căn cứ vào n ng độ chuẩn được xác định khi th c hiện x t nghiệm với 7 mẫu IL-2R đã được chuẩn bị, thiết l p đường cong chuẩn.
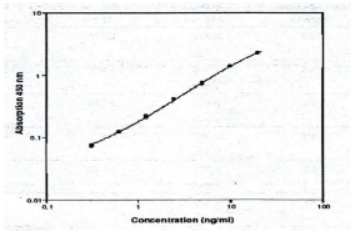
- Giá trị biện luận: D a trên đường cong chuẩn được thiết l p, tính toán giá trị IL-2R của mẫu huyết thanh.
- Giá trị IL-2R > 2400U/l có ý ngh a trong việc chẩn đoán xác định hội chứng thực bào tế bào máu.
VII. NHỮNG SAI SÓT VÀ XỬ TRÍ
- Sai sót mẫu bệnh phẩm: tên người bệnh trên giấy chỉ định xét nghiệm và trên ống máu không thống nhất, máu bị đông.
- Xử trí: yêu cầu nơi đưa mẫu xác minh lại thông tin trên giấy chỉ định và trên ống nghiệm, nếu cần phải lấy lại mẫu bệnh phẩm.
- Sai sót do nhỏ mẫu vào phiến phản ứng không thống nhất thông tin về thứ tự người bệnh và thứ tự mẫu phân tích.
- Xử trí: Vẽ sơ đồ nhỏ mẫu trước khi làm xét nghiệm. Kiểm tra đối chiếu thông tin vị trí như mẫu trước khi nhỏ mẫu.
- Chứng dương âm tính hoặc chứng minh dương tính: Nếu xảy ra hiện tượng này đều không dùng được kết quả của lần xét nghiệm này. Nguyên nhân có thể do hóa chất không đảm bảo chất lượng, do không thực hiện đủ và đúng các bước trong quy trình xét nghiệm, nhiệt độ phản ứng không phù hợp, thực hiện bước rửa kém hiệu quả.
- Xử trí: làm lại xét nghiệm, kiểm tra chỉ dùng hóa chất c n hạn sử dụng và được bảo quản đúng điều kiện theo hướng đãn của nhà sản xuất, tuân thủ đúng các bước quy trình, kiểm soát tốt nhiệt độ phòng xét nghiệm (25-30oC).
Hướng dẫn chẩn đoán và điều trị một số bệnh thường gặp ở trẻ em - Bộ y tế 2015
Hướng dẫn quy trình kỹ thuật chuyên ngành Hóa sinh - Bộ y tế 2018
Hướng dẫn quy trình kỹ thuật chuyên ngành Huyết học - Truyền máu - Miễn dịch - Dị ứng - Sinh học phân tử - Bộ y tế 2017
Hướng dẫn chẩn đoán và điều trị một số bệnh về Răng hàm mặt - Bộ y tế 2015
Hướng dẫn quy trình kỹ thuật ngoại khoa chuyên khoa phẫu thuật tiết niệu - Bộ y tế 2017
Ung thư bàng quang là bệnh ung thư bắt đầu ở các tế bào bàng quang. Ước tính có khoảng hàng trăm ngàn ca mắc mới ung thư bàng quang trên thế giới mỗi năm. Nam giới có tỷ lệ mắc ung thư bàng quang phổ cao hơn phụ nữ. Có nhiều phương pháp điều trị bệnh ung thư bàng quang, một trong số đó là liệu pháp miễn dịch, một phương pháp điều trị có tác dụng tăng cường phản ứng của hệ miễn dịch với tế bào ung thư.
Có nhiều phương pháp điều trị ung thư biểu mô tế bào thận di căn, gồm có phẫu thuật, liệu pháp nhắm trúng đích và hóa trị. Nhưng không phải khi nào cũng có thể điều trị bệnh bằng liệu pháp nhắm trúng đích. Nguyên nhân có thể là do bệnh ung thư không đáp ứng tốt với liệu pháp nhắm trúng đích hoặc các loại thuốc nhắm trúng đích gây ra tác dụng phụ hay phản ứng dị ứng nghiêm trọng. Trong những trường hợp này, bác sĩ có thể chỉ định một phương pháp điều trị khác là liệu pháp miễn dịch.
Liệu pháp miễn dịch là một phương pháp điều trị ung thư, trong đó sử dụng các loại thuốc có tác dụng tăng cường khả năng chống lại các tế bào bất thường của hệ miễn dịch. Liệu pháp miễn dịch đã được sử dụng cho nhiều bệnh ung thư, trong đó có cả ung thư thận.
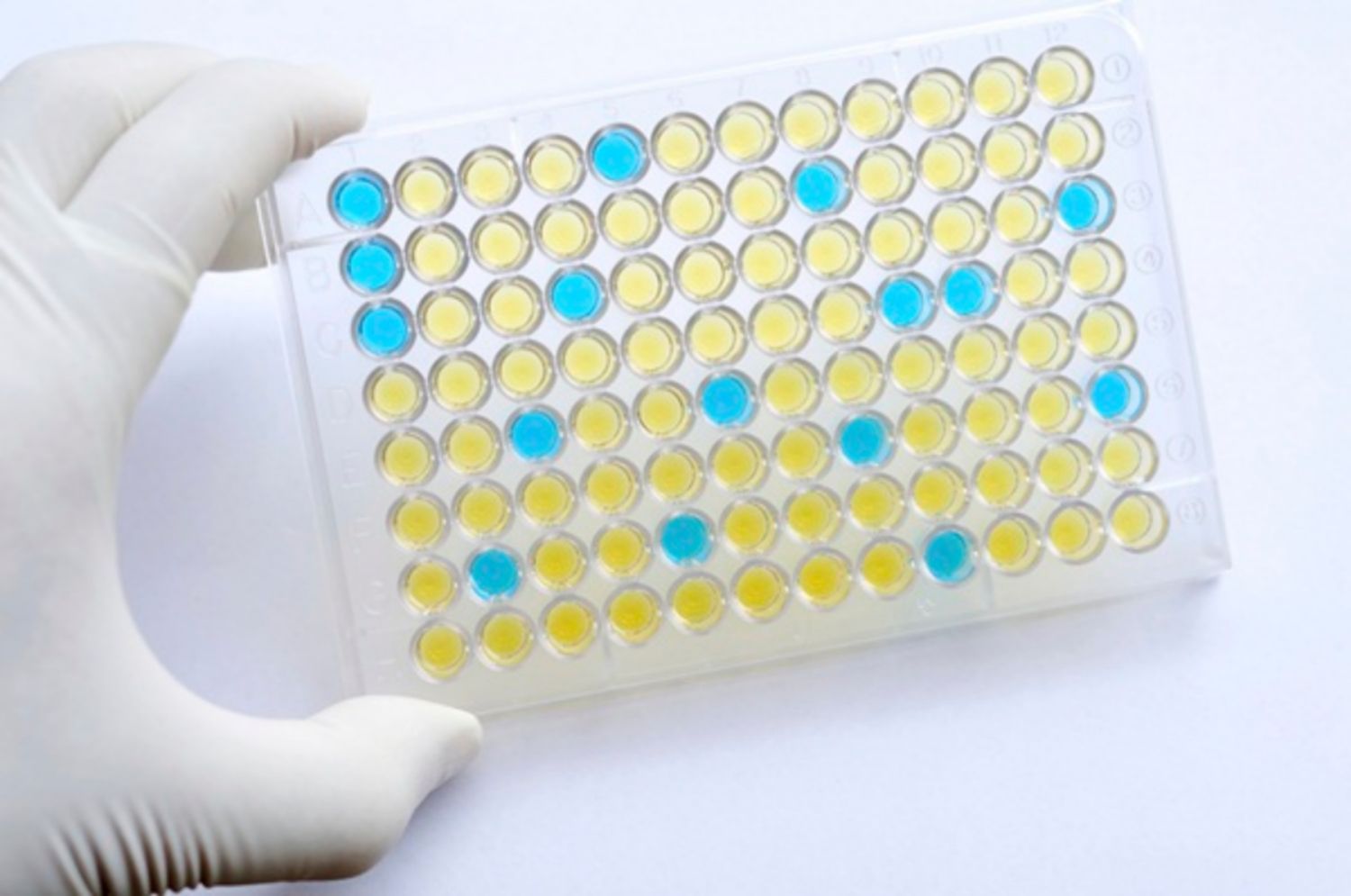
Xét nghiệm ELISA được khuyến nghị cho những trường hợp đã phơi nhiễm với HIV hoặc có nguy cơ bị lây nhiễm HIV.
Trong khi nguyên nhân chính xác của bệnh chàm không được biết, các nhà nghiên cứu hiểu rằng hệ miễn dịch có liên quan.
- 1 trả lời
- 2537 lượt xem
Bé nhà em sinh mổ mới được 20 ngày tuổi. Bé bị thiếu men G6PD. Hai vợ chồng em không ai bị, vậy sao bé nhà em lại bị thiếu men G6PD vậy bác sĩ? Em có cần cho bé đi xét nghiệm lại cho chuẩn xác không ạ? Ngoài ra, sữa của em không nhiều. Tìm hiểu sản phẩm lợi sữa Mabio thì em thấy có các thành phần là chè vằng, hương nhu, cao tàu bay, ích mẫu, bạch biển súc. Bác sĩ cho em hỏi, khi đang cho con bú thì các thành phần này có gây hại cho sức khỏe của bé không ạ?
- 1 trả lời
- 1759 lượt xem
- Bác sĩ cho tôi hỏi, bé nhà tôi có cần phải tiêm liều vắc xin bổ sung nhắc lại không, nếu xét nghiệm máu cho thấy bé đã miễn dịch với bệnh? Cảm ơn bác sĩ!
- 1 trả lời
- 1359 lượt xem
- Thưa bác sĩ, việc sử dụng nhiều hơn một mũi vắc -xin cùng lúc, liệu có gây quá tải cho hệ miễn dịch của bé không ạ?
- 1 trả lời
- 772 lượt xem
Em đang mang thai và làm xét nghiệm huyết đồ có chỉ số như sau: LYM: 17.68 %L RBC: 4.9 M/uL HGB: 103.4 g/l MCV: 72.08 fL MCH: 21.1 pg. Kết quả phết máu ngoại biên: kích thước hồng cầu nhỏ. Bs yêu cầu kiểm tra máu chồng và làm thêm xét nghiệm máu vợ. Kết quả máu chồng bình thường. Chỉ số máu vợ như sau: Chỉ số Ferritin: 61.01 ng/ ml. Kết quả điện di Hb: Hb A: 92.7% Hb A2: 5.5% Hb F: 1.8%. Như vậy, có đúng là em bị bệnh thiếu máu tán huyết không? Và, em có nên uống viên bổ sung sắt không ạ?
- 1 trả lời
- 2219 lượt xem
Em đi khám, bs kết luận là thai khoảng 34 tuần, đường kính lưỡng đỉnh và cân nặng 2.220g của bé nhỏ hơn tuổi thai. Có thể là tuổi thai của em tính chưa chính xác. Nhưng nếu như vậy, có phải là thai nhi phát triển không bằng tuổi thai thật và bé bị thiếu dưỡng chất phải không ạ?