Nghiên cứu: Đánh giá các kỹ thuật lấy mỡ, xử lý và tiêm trong cấy mỡ tự thân
Tóm lược
Bối cảnh
Hiện nay, phương pháp cấy mỡ tự thân hay tiêm mỡ tự thân để cải thiện kích thước hay đường nét cho nhiều bộ phận, vị trí trên cơ thể, ví dụ như nâng ngực, đang ngày càng nhận được nhiều sự quan tâm. Tuy nhiên, phương pháp này có nhiều kỹ thuật thực hiện khác nhau và mỗi kỹ thuật đem lại mức độ hiệu quả cũng như là tỷ lệ tái hấp thu mỡ không giống nhau.
Phương pháp
Các tác giả chọn ra những nghiên cứu tiêu biểu về ảnh hưởng của quy trình lấy (hút) mỡ, kỹ thuật xử lý và phương pháp tiêm đối với khả năng tồn tại của mỡ sau khi cấy. Bản đánh giá này tập trung vào tác động của các kỹ thuật khác nhau từ kết quả quan sát được qua các phương pháp: phân tích trong ống nghiệm, thử nghiệm trên động vật và thử nghiệm trên người.
Kết quả
Các nghiên cứu trong bản đánh giá này cho thấy hiệu quả của các kỹ thuật khác nhau. Không có sự khác biệt nào đáng kể về tỷ lệ mỡ tồn tại sau khi cấy giữa các vị trí lấy mỡ, các kỹ thuật chuẩn bị vị trí lấy mỡ, kỹ thuật lấy mỡ, kích thước ống thông hút mỡ hoặc tốc độ ly tâm khi sử dụng dung dịch tumescent. Kỹ thuật xử lý qua gạc (gauze rolling) đã được chứng minh là có tác dụng tăng cường thể tích mỡ, trong khi đó, các thử nghiệm trên động vật cho thấy không có sự khác biệt nào đáng kể về tỷ lệ mỡ tồn tại của phương pháp ly tâm, tinh lọc hoặc lắng đọng. Ngược lại, các thử nghiệm lâm sàng ở người đã cho thấy khi mỡ được xử lý bằng phương pháp ly tâm thì cho kết quả cao hơn so với phương pháp lắng đọng. Ngoài ra, tỷ lệ mỡ tồn tại sau khi cấy sẽ cao hơn nếu tốc độ quay ly tâm chậm, và tiêm vào những khu vực ít cử động.
Kết luận
Ngày càng có nhiều nghiên cứu được tiến hành nhằm xác định các phương pháp giúp nâng cao tỷ lệ tồn tại của mỡ sau khi cấy. Mặc dù có một số khác biệt giữa các kỹ thuật lấy và cấy mỡ khi được thực hiện trong phòng thử nghiệm nhưng những kết quả nghiên cứu này là chưa đủ để ứng dụng vào quy trình cấy mỡ trong thực tiễn. Do đó sẽ cần thêm các nghiên cứu bổ sung được thực hiện trên người để hỗ trợ phát triển một quy trình cấy mỡ tự thân tiêu chuẩn.
Giới thiệu
Cấy mỡ tự thân đã trở thành một phương pháp phổ biến để chỉnh sửa kích thước và đường nét cho nhiều vị trí khác nhau của cơ thể trong phẫu thuật thẩm mỹ và phẫu thuật tái tạo. Một cuộc khảo sát gần đây cho thấy khoảng 80% các bác sĩ phẫu thuật thẩm mỹ đã sử dụng phương pháp cấy mỡ tự thân cho khách hàng của mình. Phương pháp cấy mỡ tự thân đã được sử dụng để cải thiện các đường nét trên khuôn mặt, nâng ngực, phục hồi tổn thương do xạ trị, điều trị co thắt bao xơ sau nâng ngực bằng túi độn, chỉnh sửa biến dạng sau chấn thương, dị tật bẩm sinh và phục hồi những vùng bị bỏng.
Cấy mỡ tự thân có một số ưu điểm như không kích thích đáp ứng miễn dịch, quy trình thực hiện đơn giản, chi phí thấp và dễ tiếp cận. Mỡ để cấy được hút từ những vùng có mỡ thừa, qua xử lý và được tiêm vào vị trí cần. Mỡ sau khi hút gồm có các tế bào mỡ và tế bào tạo mạch nền (stromal vascular fraction cell), bao gồm tế bào gốc thu từ mô mỡ, nguyên bào mỡ (preadipocyte), nguyên bào sợi, tế bào nội mô mạch máu và nhiều loại tế bào miễn dịch. Nhiều nghiên cứu chuyên sâu đã chỉ ra rằng các tế bào tạo mạch nền và tế bào gốc thu từ mô mỡ có thể cải thiện khả năng tồn tại của mỡ sau khi cấy nhờ các đặc tính tạo mạch của chúng.
Mặc dù cấy mỡ tự thân hiện nay là một kỹ thuật phổ biến được sử dụng bởi nhiều bác sĩ thẩm mỹ, nhưng phải đến năm 1980 thì phương pháp này mới được ứng dụng rộng rãi. Các báo cáo ban đầu về cấy mỡ tự thân của Neuber, Czerny và Holländer đã cho thấy kết quả tự nhiên, tích cực khi phương pháp này được sử dụng cho khuôn mặt và ngực. Tuy nhiên, sau những thành công ban đầu này, các nghiên cứu tiếp theo đã cho thấy các mức độ thất bại khác nhau khi cấy mỡ tự thân mà vấn đề chủ yếu là tình trạng bất cân đối do tái hấp thu mỡ.
Kể từ đầu những năm 1980, nhiều báo cáo nghiên cứu đã cho thấy kết quả tích cực của phương pháp cấy mỡ tự thân, và sau đó, phương pháp này lại trở nên phổ biến một lần nữa. Nhiều nghiên cứu sau khi gặp thất bại trong những lần thử nghiệm ban đầu đã chỉ ra tầm quan trọng của các kỹ thuật được sử dụng đối với kết quả lâu dài.
Trong bản đánh giá này, chúng tôi tóm tắt nội dung của các báo cáo nghiên cứu mô tả những phương pháp lấy mỡ, xử lý và tiêm khác nhau. Những nghiên cứu này đã mở rộng tầm hiểu biết của chúng tôi về các phương pháp cải thiện kết quả lâu dài khi cấy mỡ tự thân.
Vị trí lấy mỡ
Mặc dù vị trí lấy mỡ sẽ phụ thuộc vào những vùng có mỡ thừa của từng người nhưng việc xác định được những vị trí lấy mỡ tối ưu sẽ giúp chọn ra kỹ thuật thực hiện phù hợp (Bảng 1).
Rohrich và cộng sự đã không nhận thấy có sự khác biệt đáng kể nào về khả năng sống sót của tế bào mỡ được lấy từ bụng, eo, đùi và đầu gối khi dùng ống thông cầm tay.
Ullmann và cộng sự đã thử tiêm mỡ được lấy từ bụng, ngực và đùi vào chuột rồi quan sát thì thấy không có sự khác biệt đáng kể về thể tích mỡ.
Li và các đồng nghiệp đã thử tiêm mỡ được lấy từ eo, bụng trên, bụng dưới, đùi sau và đùi trong vào chuột và cũng không nhận thấy có sự khác biệt lớn nào về thể tích hay các thông số mô học kể cả sau 12 tháng từ thời điểm cấy.
Bảng 1.
Các nghiên cứu đánh giá sự khác biệt giữa các vị trí lấy mỡ
Các thử nghiệm ở người cũng đã cho thấy rằng không có sự khác biệt nào đáng kể về khả năng duy trì thể tích sau cấy mỡ khi dùng mỡ lấy từ bụng và các vị trí khác. Mỡ được lấy từ các vị trí này đều cho kết quả tạo nét và chỉnh sửa sự không cân xứng tương đương nhau ở những người bị chứng nhỏ nửa mặt hay hội chứng Treacher Collins. Trong trường hợp nâng ngực, mỡ được lấy từ bụng và đùi cũng không cho thấy sự khác biệt lớn về thể tích mỡ cấy. Tuy nhiên, mô mỡ lấy từ đùi có tính nguyên vẹn cấu trúc cao hơn, ít hình thành cục cứng hơn, nguy cơ hoại tử và xơ hóa thấp hơn, trong khi đó mô mỡ lấy từ bụng có lại có khả năng hình thành mạch máu cao hơn.
Tính nguyên vẹn cấu trúc và hiện tượng hình thành mạch máu này có thể những đặc điểm góp phần làm cho tế bào mỡ được lấy từ đùi trong và bụng có khả năng tồn tại cao hơn so với mỡ ở các vùng khác. Tuy nhiên, các nghiên cứu cho đến thời điểm hiện tại cho thấy rằng không có sự khác biệt đáng kể nào về thể tích mỡ sau khi cấy giữa các vị trí lấy mỡ khác nhau.
Kỹ thuật chuẩn bị vị trí lấy mỡ
Kỹ thuật gây tê bằng dung dịch tumescent (tumescent anesthesia) ban đầu được phát triển dành cho quy trình hút mỡ với phương pháp gây tê tại chỗ, và nhiều lợi ích của việc sử dụng dung dịch tumescent đã được chứng minh, gồm có giảm đau, giảm mất máu và giúp cho quá trình hút mỡ được dễ dàng hơn. Tuy nhiên, không rõ liệu việc bơm dung dịch tumescent trước khi hút mỡ có ảnh hưởng xấu đến sự tồn tại của mỡ sau khi cấy hay không (Bảng 2).
Agostini và các đồng nghiệp đã chứng minh rằng việc sử dụng dung dịch tumescent làm tăng khả năng tồn tại của tế bào mỡ so với kỹ thuật hút mỡ khô (dry technique). Sự tiếp xúc với epinephrine và lidocaine trong dung dịch tumescent không làm thay đổi vĩnh viễn các chức năng của mô mỡ hay hoạt động trao đổi chất của tế bào mỡ. Hơn nữa, việc bơm dung dịch tumescent cũng không ảnh hưởng đáng kể đến thể tích mỡ cấy hay cấu trúc mô học.
Nghiên cứu phân tích các loại thuốc gây tê khác nhau đã chứng minh rằng khi mô mỡ được tiếp xúc với bupivacaine, mepivacaine, ropivacaine và lidocaine thì khả năng tồn tại của tế bào gốc thu từ mô mỡ sẽ cao hơn so với khi dùng kết hợp articaine và epinephrine. Epinephrine có thể ảnh hưởng đến thụ thể α 1 trên các mô xung quanh tế bào mỡ được cấy. Nhìn chung, kỹ thuật hút mỡ tumescent giúp làm tăng khả năng sống của tế bào mỡ so với kỹ thuật hút mỡ khô và không có sự khác biệt đáng kể nào giữa các loại thuốc gây tê thường được sử dụng, ngoại trừ articaine và epinephrine. Rất khó để đưa ra cơ chế lý giải tại sao khả năng tồn tại của mỡ tự thân lại tăng lên sau khi tiếp xúc trong thời gian ngắn với các loại thuốc gây tê tại chỗ. Tuy nhiên, dựa trên các nghiên cứu hiện tại, việc sử dụng dung dịch tumescent tại thời điểm hút mỡ không gây tác động nào bất lợi đến khả năng tồn tại của tế bào mỡ và thậm chí còn có thể làm tăng khả năng sống.
Bảng 2:
Các nghiên cứu đánh giá sự khác biệt giữa các phương pháp chuẩn bị vị trí lấy mỡ
Phương pháp lấy mỡ
Các nghiên cứu đánh giá tác động của kỹ thuật hút mỡ bằng ống thông cầm tay, bằng máy hút và bằng sóng siêu âm đã chứng minh sự khác biệt về khả năng sống sót và chức năng của tế bào mỡ (Bảng 3).
Chức năng của tế bào mỡ được phân tích bằng xét nghiệm enzyme glycerol-3- phosphate dehydrogenase – phương pháp đánh giá mức độ thẩm thấu của enzyme này qua màng sinh chất trong trạng thái tổn thương tế bào.
Về mặt mô học, mô mỡ được lấy bằng kỹ thuật hút mỡ bằng máy hút và sóng siêu âm không cho thấy dấu hiệu bị tổn thương tế bào và về mặt sinh lý, mỡ được lấy bằng cả hai kỹ thuật này đều có thể dùng được và có hoạt động enzyme bình thường.
So với kỹ thuật hút mỡ bằng máy hút, một số nghiên cứu đã chỉ ra rằng kỹ thuật hút mỡ bằng ống thông cầm tay giúp giữ được số lượng tế bào mỡ và khả năng sống sót cao hơn. Tuy nhiên, khi sử dụng dung dịch tumescent thì không có sự khác biệt đáng kể nào về số lượng tế bào mỡ hoặc khả năng sống sót giữa kỹ thuật dùng ống thông cầm tay và hút mỡ bằng máy hút.
Để đánh giá thêm về tác động của ống thông cầm tay, kỹ thuật hút mỡ bằng máy hút và bằng sóng siêu âm, mỡ sau khi được lấy bằng các kỹ thuật này đã được tiêm vào những con chuột bị suy giảm miễn dịch. Kết quả cho thấy không có sự khác biệt lớn nào về thể tích mỡ giữa các phương pháp này. Kết quả các nghiên cứu này cho thấy phương pháp được sử dụng để hút mỡ có vai trò không quá quan trọng vì dù dùng phương pháp nào thì tỷ lệ sống sót của tế bào mỡ cũng tương đương nhau. Tuy nhiên, những nghiên cứu này chỉ theo dõi trong thời gian ngắn sau khi tiêm mỡ vào chuột (4, 6 hoặc 12 tuần) nên chưa thể đánh giá khả năng duy trì về lâu dài. Vì sau khi cấy, mỡ tự thân có thể tồn tại trong cơ thể suốt nhiều năm nên sẽ cần thêm các nghiên cứu bổ sung với thời gian theo dõi dài hơn 12 tuần để có bằng chứng đánh giá tác động của các phương pháp hút mỡ khác nhau đối với kết quả về lâu dài.
Bảng 3
Các nghiên cứu đánh giá sự khác biệt giữa các kỹ thuật hút mỡ
Chú thích: G3PDH: glycerol-3-phosphate dehydrogenase
PPAR-γ: thụ thể kích hoạt peroxisome proliferator-γ
SVF: tế bào tạo mạch nền
Kích thước ống thông hút mỡ
Các nghiên cứu sau khi đánh giá sự khác biệt giữa các kích thước ống thông hút mỡ đã chỉ ra rằng việc sử dụng ống thông có đường kính lớn hơn sẽ làm tăng khả năng sống của tế bào mỡ (Bảng 4).
Erdim và cộng sự đã chứng minh rằng khả năng tồn tại của tế bào mỡ được hút bằng ống thông 6mm là cao hơn so với ống thông 2mm và 4mm. Sau khi thực hiện thử nghiệm trên chuột và đánh giá sau 6 tuần, Kirkham và các đồng nghiệp đã cho thấy rằng mỡ được hút bằng ống thông kích thước lớn (đường kính 5mm) có khả năng hình thành vùng mỡ sau cấy lớn hơn ống thông kích thước nhỏ. Kết quả nghiên cứu này cho thấy tính nguyên vẹn của mô mỡ tăng lên, khả năng xảy ra đáp ứng miễn dịch và hiện tượng xơ hóa thấp hơn so với mỡ được hút bằng ống thông 3mm. Tuy nhiên, cần lưu ý rằng, trong các nghiên cứu này, mỡ được lấy mà không dùng dung dịch tumescent. Sẽ cần thêm nghiên cứu về tác động của kích thước ống thông đối với quá trình hút mỡ sử dụng dung dịch tumescent. Ngoài kích thước ống thông, các nghiên cứu còn so sánh ống thông nhiều lỗ với ống thông Coleman 3mm và cho thấy rằng không có sự khác biệt đáng kể về khả năng tồn tại của tế bào mỡ hay diện tích của vùng mỡ sau cấy.
Bảng 4.
Các nghiên cứu đánh giá sự khác biệt giữa các kích thước ống thông
Các phương pháp xử lý mỡ sau hút
Các nghiên cứu đã đánh giá tác động của các kỹ thuật xử lý mô mỡ sau hút khác nhau, gồm có ly tâm, tách bằng trọng lực, rửa và lọc đối với khả năng tồn tại của tế bào mỡ sau cấy (Bảng 5).
Khảo sát đã đưa ra kết luận rằng trong số các bác sĩ thẩm mỹ thực hiện phương pháp cấy mỡ tự thân thì 34% sử dụng kỹ thuật ly tâm, 45% sử dụng kỹ thuật tách bằng trọng lực, 34% sử dụng kỹ thuật lọc, 11% sử dụng kỹ thuật xử lý qua gạc, 3% không xử lý mô mỡ trước khi tiêm và 7% sử dụng một số kỹ thuật khác. Việc sử dụng một kỹ thuật xử lý tối ưu sẽ làm tăng số lượng tế bào mỡ sống sót và cuối cùng là tăng lượng mỡ và khả năng duy trì kết quả về lâu dài.
Bảng 5.
Nghiên cứu đánh giá sự khác biệt giữa các kỹ thuật xử lý mỡ sau hút
Các nghiên cứu cũng chỉ ra rằng kỹ thuật xử lý nào có thể duy trì mật độ cao các tế bào tạo mạch nền và tế bào gốc từ mỡ thì sẽ có thể tăng cường khả năng sống sót của mỡ sau cấy; do đó, các phương pháp xử lý cần được thực hiện một cách tối ưu sao cho có thể giữ tối đa số lượng tế bào tạo mạch nền và tế bào gốc từ mỡ. Gần đây, các nghiên cứu đã chỉ ra rằng kỹ thuật xử lý bằng gạc cotton làm tăng khả năng sống sót của tế bào mỡ và diện tích vùng mỡ cấy so với kỹ thuật quay ly tâm, lọc và rửa. Những tế bào tạo mạch nền và tế bào gốc từ mỡ này đã được chứng minh là làm tăng thể tích mỡ cấy bằng cách tăng cường sự hình thành mạch máu và sự biệt hóa của quá trình tạo mỡ. Các nghiên cứu trên động vật sống cũng chỉ ra rằng phương pháp xử lý bằng gạc cotton cho diện tích vùng mỡ cấy lớn nhất và khả năng duy trì cấu trúc mỡ sau cấy cao nhất. Tuy nhiên, lý do tại sao phương pháp xử lý bằng gạc cottong lại có ưu điểm như vậy vẫn chưa được làm rõ.
Trong các nghiên cứu trên động vật, phương pháp xử lý mỡ sau hút bằng cách lọc và quay ly tâm cho diện tích mỡ cấy nhỏ hơn. Tương tự, nhiều nghiên cứu cũng chứng minh rằng phương pháp quay ly tâm và rửa làm giảm sự tăng sinh tế bào, giảm số lượng tế bào mỡ có nhân và giảm sự nguyên vẹn cấu trúc. Rất có thể quá trình lọc hoặc tốc độ ly tâm cao là nguyên nhân gây nên những tổn hại cho mô mỡ. Tốc độ quay ly tâm và mật độ các tế bào có thể làm giảm kích thước vùng mỡ cấy và điều này sẽ được thảo luận trong các phần sau. Khi so sánh giữa các phương pháp quay ly tâm, lọc và lắng đọng trong các thử nghiệm trên động vật thì không có sự khác biệt nào đáng kể về trọng lượng hay cấu trúc của các vùng mỡ cấy.
Ngược lại, các nghiên cứu được thực hiện ở người đã chứng minh phương pháp quay ly tâm cho kết quả khả quan hơn so với phương pháp tách bằng trọng lực. Butterwick đã chứng minh phương pháp tiêm mỡ tự thân sau khi xử lý bằng kỹ thuật ly tâm cho hiệu quả làm đầy và mịn mu bàn tay cao hơn so với kỹ thuật tách bằng trọng lực. Các nghiên cứu so sánh tác động của quá trình xử lý mỡ bằng kỹ thuật quay ly tâm, rửa và lọc cho thấy rằng không có sự khác biệt nào đáng kể về tỷ lệ sống sót của mỡ; tuy nhiên, kỹ thuật lọc gây hình thành nốt sần, trong khi kỹ thuật quay ly tâm thì không. Tóm lại, mặc dù đã có nhiều nghiên cứu được thực hiện nhưng kết quả thử nghiệm ở người và ở động vật vẫn chưa có sự nhất quán. Do đó vẫn chưa thể kết luận phương pháp xử lý mỡ nào là ưu việt nhất mà sẽ cần thêm các nghiên cứu bổ sung để xác định một kỹ thuật tối ưu.
Tốc độ/lực ly tâm
Lực ly tâm cũng là một yếu tố ảnh hưởng đến kết quả của phương pháp cấy mỡ tự thân.
Tương tự như mức áp suất âm trong phương pháp hút mỡ bằng máy hút, áp lực dương trong quá trình ly tâm có thể tác động đáng kể đến kết quả (Bảng 6).
Ferraro và cộng sự đã chứng minh rằng ly tâm với lực lớn hơn 50g sẽ gây tổn hại đến sự nguyên vẹn cấu trúc của mô mỡ, tăng nguy cơ hoại tử và chết tế bào, giảm khả năng biệt hóa trong quá trình tạo mỡ và giảm sự hình thành tiểu thùy mỡ. Sự hình thành tiểu thùy mỡ trong quá trình tạo mạch máu có vai trò cung cấp máu và chất dinh dưỡng cho mô mỡ và cuối cùng duy trì vùng mỡ cấy để kết quả được lâu dài. Tốc độ ly tâm càng cao thì sẽ càng làm tăng tỷ lệ chất dịch, mỡ lỏng, giảm thể tích mô mỡ có thể tổn tại và tăng nguy cơ tổn thương tế bào mỡ. Tuy nhiên, khi thử nghiệm trên chuột và quan sát tại thời điểm 4 tuần sau khi tiêm thì quá trình ly tâm với lực lên đến 4200g cũng không ảnh hưởng đến số lượng tế bào tạo mạch nền có thể tồn tại hoặc trọng lượng của vùng mỡ cấy. Lee và cộng sự đã tiến hành thử nghiệm trên chuột và đánh giá sau 4 tuần kể từ thời điểm tiêm thì thấy rằng mỡ được xử lý bằng phương pháp ly tâm với lực 10.000g cho hiệu quả cao nhất. Nguyên nhân dẫn đến sự khác biệt giữa các nghiên cứu có thể là do sử dụng loại máy ly tâm khác nhau và thời gian mà mô mỡ được quay ly tâm không giống nhau. Hơn nữa, kỹ thuật hút mỡ bằng máy hút có thể làm tăng khả năng tổn thương mô mỡ và việc xử lý bằng phương pháp quay ly tâm lại càng khiến cho mô mỡ bị tổn hại nặng hơn.
Bảng 6.
Các nghiên cứu về sự khác biệt giữa các mức tốc độ/lực ly tâm
Ngược lại, các nghiên cứu đánh giá tác động của quá trình ly tâm sau khi hút mỡ bằng ống thông cầm tay cho thấy tốc độ ly tâm (92 đến 20.627g) không ảnh hưởng lớn đến khả năng tồn tại của tế bào mỡ hoặc trọng lượng của vùng mỡ cấy. Trên thực tế, lực ly tâm càng cao thì lượng mảnh vụn và tạp chất trong mỡ càng thấp. Những phát hiện này cho thấy rằng quá trình ly tâm sau khi hút mỡ bằng ống thông cầm tay là điều cần thiết để loại bỏ các mảnh vụn mô và ngăn ngừa hiện tượng xơ hóa trong vùng mỡ cấy. Những kết quả nghiên cứu này còn cho thấy rằng so với hút mỡ bằng máy hút thì phương pháp hút mỡ bằng ống thông cầm tay làm giảm khả năng tổn thương mô mỡ, do đó mà mô mỡ có thể chịu được tốc độ ly tâm cao hơn mà không bị tổn thương tế bào.
Mật độ mô sau xử lý
Các nghiên cứu cũng chỉ ra rằng quá trình ly tâm sẽ cho ra mật độ tế bào khác nhau trong các lớp mỡ được tiêm (Bảng 7). Nhiều nghiên cứu trước đây đã chứng minh lớp bên dưới có mật độ tế bào mỡ có thể tồn tại cao nhất (mỡ mật độ cao) và lớp bên trên lại có số lượng tế bào có thể tồn tại thấp nhất (mỡ mật độ thấp) (Hình 1). Hơn nữa, nghiên cứu cho thấy, tiêm mỡ mật độ cao vào những con chuột FVB/NJ có hệ miễn dịch bình thường cho kết quả cao nhất sau 2 đến 10 tuần kể từ khi tiêm. Đánh giá mô học trên vùng được cấy mỡ sau khi tiêm mỡ mật độ cao cho thấy số lượng tế bào nội mô cao hơn, số lượng dải collagen thấp hơn và giảm nguy cơ xơ hóa. Ngoài ra còn có sự gia tăng các yếu tố tạo mạch như yếu tố tăng trưởng nội mô mạch máu, yếu tố bắt nguồn từ tế bào đệm 1-alpha hay SDF-1α (stromal cell - derived factor 1alpha) , yếu tố tăng trưởng có nguồn gốc tiểu cầu và adiponectin. Để tăng cường khả năng sống sót và duy trì kết quả sau tiêm mỡ mật độ thấp, Butala và đồng nghiệp đã xử lý mỡ mật độ thấp với plerixafor (AMD3100) - một chất kích thích miễn dịch mà trước đây đã được chứng minh là có thể huy động các tế bào gốc tạo máu (hematopoi-etic stem cell) và hỗ trợ quá trình tạo mạch máu. Vùng mỡ mật độ thấp qua xử lý bằng AMD3100 có kích thước tương đương với vùng mỡ mật độ cao, cho thấy rằng mỡ mật độ thấp cũng có thể tạo ra kết quả tương đương, với điều kiện là huy động được các tế bào gốc trung mô vào mô mỡ. Những nghiên cứu này cũng cho thấy tầm quan trọng của phản ứng ở cơ thể người được tiêm đối với khả năng chữa lành và duy trì mô mỡ tự thân sau khi cấy.
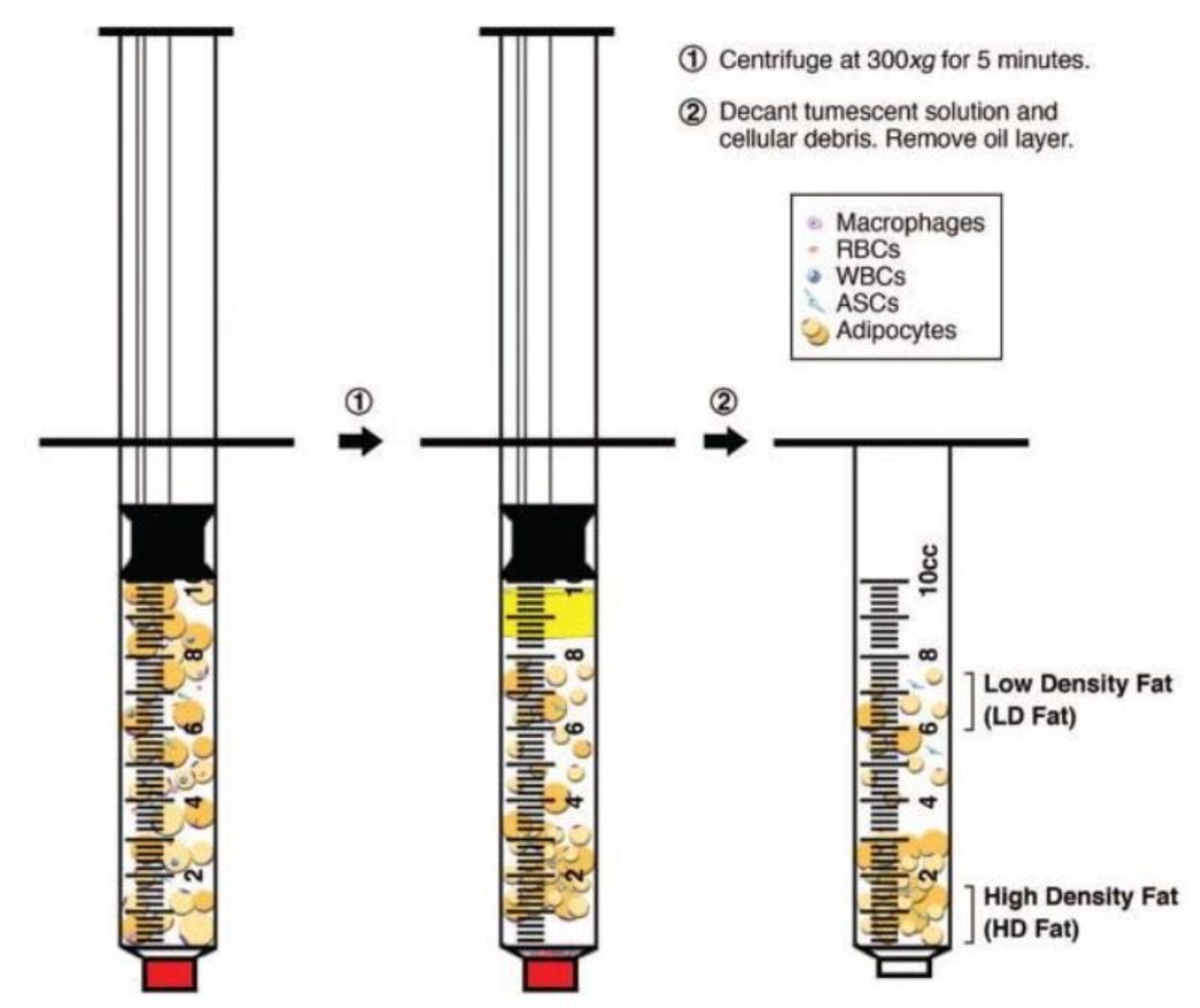
Chú thích:
Low density fat: mỡ mật độ thấp
High density fat: mỡ mật độ cao
Quay ly tâm với lực 3000g trong 5 phút
Lọc dung dịch tumescent và vụn tế bào. Loại bỏ lớp mỡ lỏng
Macrophage: đại thực bào
RBC: Hồng cầu
WBC: Bạch cầu
Adipocyte: Tế bào mỡ
Bảng 7.
Nghiên cứu về sự khác biệt giữa các mật độ mô mỡ sau ly tâm
Chú thích: Tế bào SVF: tế bào tạo mạch nền
VEGF: yếu tố tăng trưởng nội mô mạch máu
PDGF- β: yếu tố tăng trưởng có nguồn gốc tiểu cầu- β
SDF-1α: yếu tố bắt nguồn từ tế bào đệm 1-alpha (stromal cell–derived factor 1-alpha)
Quá trình tiêm
Quá trình tiêm mỡ tự thân đã qua xử lý vào vị trí cần tiêm đòi hỏi phải thật cẩn thận để cho ra kết quả mong muốn, đặc biệt là với các trường hợp cần chỉnh sửa đường nét trên khuôn mặt (Bảng 8). Coleman đã mô tả quá trình tiêm mỡ tự thân đã qua xử lý bằng ống tiêm Luer-Lok được nối với kim đầu tù cannula 17G. Theo Coleman, chỉ nên tiêm mỡ trong khi rút kim đầu tù cannula để mô mỡ đi vào các mặt phẳng mô tự nhiên. Tốc độ tiêm chậm 0.5 đến 1.0 ml/giây sẽ tạo vùng mỡ cấy lớn hơn so với tốc độ tiêm nhanh từ 3.0 đến 5.0 ml/giây. Việc tăng tốc độ tiêm có thể dẫn đến tổn thương tế bào do ứng suất trượt, tích tụ collagen và thâm nhiễm miễn dịch nhiều hơn trong các vùng mô cấy.
Bảng 8.
Các nghiên cứu về tác động của kỹ thuật tiêm
Các vị trí nhận mỡ
Các nghiên cứu đã đánh giá sự khác biệt về hiệu quả của phương pháp cấy mỡ tự thân tại những vị trí nhận mỡ khác nhau. Các nghiên cứu ở thỏ cho thấy tiêm mỡ tự thân vào cơ cho kết quả cao hơn so với tiêm vào lớp trung bì, lý do có thể là nhờ khả năng hình thành mạch máu mới ở lớp cơ cao hơn. Tuy nhiên, Rieck và Schlaak đã chứng minh khi cấy mỡ tự thân vào cơ thì khả năng tồn tại của mỡ lại thấp hơn do cơ phải chuyển động nhiều. Những khu vực thường xuyên cử động trên khuôn mặt, chẳng hạn như giữa hai đầu lông mày và môi là những vị trí ít thay đổi hơn khi tiêm mỡ tự thân so với các khu vực ít phải cử động, chẳng hạn như hàm và má ngoài. Các yếu tố khác cũng ảnh hưởng đến kết quả sau cấy mỡ tự thân và khả năng tồn tại của mỡ là độ tuổi của khách hàng, tình trạng của vùng da bên trên và mức độ nghiêm trọng của khuyết điểm cần chỉnh sửa. Càng có tuổi thì sự đầy đặn ở nhiều vùng trên khuôn mặt sẽ càng giảm đi, các lớp mỡ dưới da cùng các cấu trúc mô mềm và xương bên dưới càng trở nên nổi rõ hơn. Rohrich và cộng sự đã chứng minh rằng việc khôi phục các vùng mỡ có chọn lọc bằng phương pháp cấy mỡ tự thân có thể chỉnh sửa các đường nét trên khuôn mặt một cách chính xác, tạo vẻ ngoài trẻ trung và tự nhiên hơn. Lão hóa còn làm giảm sự hình thành mạch máu mới và làm giảm khả năng duy trì kết quả sau cấy mỡ tự thân. Những người bị bỏng nặng hoặc khiếm khuyết, thiếu hụt các cấu trúc dưới da sẽ cần tiêm mỡ tự thân nhiều lần vì vùng nhận mỡ đã hình thành sẹo, xơ hóa và bị tổn hại. Các khiếm khuyết nghiêm trọng về cấu trúc khuôn mặt do chứng teo nhỏ nửa mặt (hemifacial atrophy) cũng có thể được khắc phục bằng phương pháp tiêm mỡ tự thân. Tuy nhiên, ở những người này thì kết quả mà phương pháp tiêm mỡ tự thân mang lại thường kém hơn so với người bình thường và sẽ cần tiêm nhiều lần để đạt được kết quả mong muốn.
Ngoài việc hiểu được sự khác biệt giữa các vị trí nhận mỡ, nghiên cứu được tiến hành bởi del Vecchio và Bucky đã chứng minh vai trò của việc chuẩn bị trước vị trí nhận mỡ đối với kết quả tiêm mỡ tự thân. Trong nghiên cứu này, những người tham gia được cho dùng áo nâng ngực trong 3 tuần trước và 3 tuần sau khi nâng ngực bằng mỡ tự thân. Điều này làm tăng khoảng trống nhu mô, giảm áp lực kẽ ở vú và giảm những đường nét không đều. Trong một nghiên cứu đa
trung tâm kéo dài 6 năm, những người có dùng áo nâng ngực trước và sau tiêm mỡ tự thân thì sẽ có kết quả cao hơn, nguy cơ hoại tử và biến chứng thấp hơn cũng như là khả năng tồn tại của mỡ sau khi cấy cao hơn. Sẽ cần thêm nghiên cứu bổ sung để chứng định xem liệu phương pháp này có áp dụng được cho các vị trí nhận mỡ khác ngoài ngực hay không.
Những điều cần cân nhắc
Mặc dù các nghiên cứu này đem lại một cái nhìn tổng quan về các yếu tố chính ảnh hưởng đến kết quả của phương pháp tiêm mỡ tự thân nhưng ngoài ra còn nhiều yếu tố khác chưa được đề cập. Điều quan trọng là phải đánh giá từng khách hàng trước khi tiến hành vì vấn đề và cấu tạo giải phẫu của mỗi người là khác nhau, những điều này đều ảnh hưởng lớn đến kết quả có được và là điều quyết định thể tích mỡ cần tiêm. Các nghiên cứu đã chỉ ra sự chênh lệch đáng kể về số lượng tế bào tạo mạch nền và tế bào gốc thu từ mô mỡ trong lượng mỡ cấy ở mỗi người, đây là điều có thể giải thích cho sự khác biệt về kết quả thu được ở những người tham gia.
Các tế bào tạo mạch nền và tế bào gốc thu từ mô mỡ gần đây đã nhận được nhiều sự chú ý vì khả năng chữa lành vết thương. Cho dù là bổ sung các tế bào tạo mạch nền hoặc tế bào gốc từ mô mỡ vào lượng mỡ cấy sau xử lý hoặc bổ sung trong quá trình ly tâm thì cả hai phương pháp này đều mang lại kết quả là vùng mỡ cấy lớn hơn và duy trì kết quả được lâu dài hơn. Gentile và các cộng sự đã chứng minh rằng ở những người được tiêm mỡ tự thân có bổ sung tế bào tạo mạch nền thì 63% lượng mỡ cấy vẫn tồn tại sau một năm trong khi tỷ lệ này ở nhóm đối chứng chỉ là 39%. Nghiên cứu về việc bổ sung tế bào gốc từ mô mỡ cũng cho kết quả tương tự. Kølle và cộng sự đã nhận thấy rằng việc bổ sung tế bào gốc vào mỡ sau xử lý đã tăng cường sự hình thành mô liên kết mới và làm giảm lượng mô hoại tử của vùng mỡ cấy. Zhu và cộng sự đã chứng minh mỡ tự thân được bổ sung tế bào gốc còn giúp duy trì kết quả lâu dài hơn và tăng sự hình thành mạch máu nhờ các yếu tố tạo mạch chính, bao gồm yếu tố tăng trưởng nội mô mạch máu, yếu tố tăng trưởng tế bào gan và yếu tố tăng trưởng giống insulin-1. Mặc dù các nghiên cứu đã cho thấy vai trò của các yếu tố tạo mạch mà tế bào gốc thu từ mô mỡ tạo ra, nhưng mới chỉ có rất ít nghiên cứu đánh giá vai trò các tế bào tạo mạch nền và tác động của nhóm tế bào hỗn hợp đối với sự hình thành mạch máu. Do đó sẽ cần thêm các nghiên cứu để xác định xem liệu bổ sung tế bào tạo mạch nền hay tế bào gốc thu từ mô mỡ sẽ tạo vùng mỡ cấy lớn hơn và thời gian duy trì lâu hơn.
Những người bị bỏng nặng hoặc thiếu hụt cấu trúc bên dưới da có thể cần tiêm nhiều lần để khắc phục tình trạng sẹo, xơ hóa và tổn thương ở vị trí nhận mỡ. Phương pháp tiêm nhiều lần sẽ có lợi cho một số trường hợp để tăng khả năng tạo mạch và kéo dài thời gian tồn tại của mỡ sau cấy. Các nghiên cứu bổ sung ở người sẽ tạo nền tảng cho phương pháp cấy mỡ tự thân trong tương lai và tăng mức độ phổ biến của phương pháp này trong thực tiễn lâm sàng.
Kết luận
Tiêm mỡ tự thân đã trở thành một phương pháp ngày một phổ biến để khắc phục các vấn đề về đường nét hay kích thước của nhiều vùng khác nhau trên cơ thể. Đã có rất nhiều nghiên cứu đưa ra các phương pháp để tăng cường khả năng tồn tại của mỡ tự thân sau cấy bằng cách nhắm đến cả tế bào mỡ và tế bào tạo mạch nền. Mặc dù vẫn có một số khác biệt giữa các kỹ thuật lấy mỡ và tiêm mỡ khi được nghiên cứu trong phòng thí nghiệm nhưng những khác biệt này vẫn chưa đủ để xây dựng một quy trình cấy mỡ tự thân tiêu chuẩn. Hơn nữa, hiện nay cũng chưa có dữ liệu cấp độ I hoặc cấp độ II để đảm bảo một khuyến nghị đồng thuận cho thực tiễn lâm sàng. Do đó, vẫn cần thêm các nghiên cứu trên người để có thể phát triển một quy trình chuẩn cho phương pháp cấy mỡ tự thân.
Bài viết nghiên cứu có thể bạn quan tâm
Tin liên quan
Hỏi đáp có thể bạn quan tâm