Bài giảng gây mê - bệnh viện 103
Vô khuẩn trong ngoại khoa
1. Đại cương:
1.1 Khái niệm:
Vô khuẩn là một nguyên tắc, một chế độ hàng đầu của ngành y tế nói chung và của ngành ngoại khoa nói riêng, nó có ý nghĩa thành bại trong công tác ngoại khoa.
Vô khuẩn trong ngoại khoa được đặt ra sau khi người ta tìm ra vi khuẩn và nhận thấy vai trò gây bệnh của chúng đối với cơ thể sau khi chúng xâm nhập được qua vết thương, vết mổ.
Một số thuật ngữ:
- Tiệt khuẩn: là các biện pháp tiêu diệt mọi hình thái của vi khuẩn bao gồm cả nha bào.
- Khử khuẩn:là phương pháp loại bỏ hầu hết các vi sinh vật gây bệnh (không nhất thiết phải loại bỏ nha bào) ra khỏi dụng cụ hoặc da của cơ thể nhằm làm cho dụng cụ đó không còn gây hại cho sức khỏe.
Có 3 mức độ khử khuẩn:
- Khử khuẩn mức độ cao: diệt mọi vi sinh vật gây bệnh trừ ô nhiễm nhiều nha bào.
- Khử khuẩn mức độ trung bình: ức chế trực khuẩn lao, các vi khuẩn dạng sinh dưỡng, hầu hết các virus, nấm nhưng không diệt được nha bào.
- Khử khuẩn mức độ thấp: có thể diệt được hầu hết các vi khuẩn, một số virus và nấm nhưng không diệt được vi khuẩn có sức đề kháng cao như trực khuẩn lao hoặc vi khuẩn dạng nha bào.
Khử khuẩn, tiệt khuẩn là tạo nên một môi trường vô khuẩn, ngăn ngừa không cho vi khuẩn xâm nhập vào cơ thể.
1.2 Những yếu tố gây nhiễm khuẩn vết mổ:
1.2.1 Không khí trong nhà mổ bị nhiễm khuẩn:
Mật độ vi khuẩn trong không khí phòng mổ cho phép là 300 vi khuẩn trong 1 mét khối không khí. Nếu cao hơn sẽ có nhiều nguy cơ nhiễm khuẩn vết mổ. Không khí trong phòng mổ có thể bị nhiễm khuẩn do nhiều yếu tố:
- Do phòng mổ lưu thông với các phòng điều trị hoặc những nơi nhiễm khuẩn khác.
- Do phòng mổ quá chật hẹp, ẩm nóng.
- Do phòng mổ đông người vào và qua lại nhiều.
1.2.2 Dụng cụ dùng trong phẫu thuật bị nhiễm khuẩn hoặc tiệt khuẩn không đạt yêu cầu.
Các dụng cụ dùng trong phẫu thuật có rất nhiều loại: đồ kim loại, đồ vải, cao su…tiếp xúc trực tiếp với vùng mổ. Nhiều loại phải dùng tái lại nhiều lần. Nếu không đảm bảo qui trình tiệt khuẩn sẽ là nguy cơ nguy hiểm gây nhiễm khuẩn vết mổ.
1.2.3 Phương tiện dụng cụ dùng trong nhà mổ cho gây mê hồi sức:
Bàn mổ, máy hút, đèn, máy thở, máy gây mê…nếu không đảm bảo tiệt trùng thường xuyên cũng là những yếu tố gây nhiễm khuẩn nhà mổ và vết mổ vì đây là những nguồn lây vi khuẩn.
1.2.4 Ý thức vô khuẩn của cán bộ y tế làm việc trong khu phẫu thuật:
Có thể coi đây là yếu tố đầu tiên có tính chất quyết định. Để làm giảm tỷ lệ mhiễm khuẩn đòi hỏi mỗi cán bộ y tế làm việc trong khu mổ phải có ý thức trách nhiệm cao
2. Các phương pháp khử khuẩn:
2.1 Phương pháp khử khuẩn bằng nhiệt
Đun sôi (100˚C): với thời gian không dưới 15 phút là một phương pháp đơn giản và đáng tin cậy nhằm ức chế các vi sinh vật, kể cả HIV, HBV và trực khuẩn lao. Nếu qui trình được kiểm soát tốt thì đây có thể coi là một qui trình khử khuẩn mức độ cao. Các dụng cụ kim loại và cao su có thể sử dụng phương pháp này.
Dụng cụ phải được rửa sạch, ngâm ngập trong nước. Thời gian khử khuẩn được tính kể từ khi nước bắt đầu sôi. Nếu nước đun chứa một lượng NaHCO3 ( nồng độ 2%) sẽ giúp ngăn ngừa quá trình ăn mòn dụng cụ khi đun sôi. Chú ý phải lấy dụng cụ ra khỏi nồi bằng một panh vô khuẩn ( hoặc để dụng cụ trong một giá đỡ khi đun) và sử dụng ngay dụng cụ sau khi khô. Nồi đun chỉ sử dụng cho mục đích khử khuẩn dụng cụ.
2.2 Phương pháp khử khuẩn bằng các chất hóa học:
Hiện nay có nhiều loại hóa chất khử khuẩn được sử dụng như cồn, các loại hợp chất chlorine, formaldehyde, glutaraldehyde, hydrogen peroxide (oxy già), iodophors, paracetic acid, phenoic, hợp chất amoni bậc 4.
Tính hữu hiệu của hoá chất phụ thuộc vào nồng độ, bề mặt của dụng cụ cần được sát khuẩn có sạch hay không, thời gian tiếp xúc với dụng cụ có đủ hay không.
2.1.1 Cồn
+ Đặc điểm:
Trong lĩnh vực y tế, hai loại cồn được sử dụng là cồn ethyl và cồn isopropyl. Cồn có khả năng diệt vi khuẩn lao, nấm, virus nhưng không diệt được bào tử vi khuẩn. Hoạt tính của cồn giảm mạnh khi pha loãng ở nồng độ dưới 50%. Cồn có nồng độ từ 60-90% có hiệu quả diệt khuẩn tốt nhất.
+ Cơ chế tác dụng:
Cồn phá hủy các enzyme khử hydro của vi khuẩn dẫn đến xuất hiện thêm một số acid amin mới, sự xuất hiện các acid amin này làm đảo lộn cấu trúc phân tử protein của vi khuẩn.
Cồn ức chế quá trình sản sinh các chất chuyển hóa cẩn thiết cho quá trình phân chia tế bào của vi khuẩn, vì thế ngoài tác dụng diệt khuẩn cồn còn có tác dụng kìm hãm sự nhân lên của vi khuẩn.
+ Cách sử dụng:
Cồn thường được sử dụng để khử khuẩn nhiệt kế, dụng cụ nội soi võng mạc. Khăn tẩm cồn được sử dụng những bề mặt nhỏ như nắp cao su, bóng ambu, dụng cụ siêu âm hoặc các dụng cụ sử dụng để pha chế thuốc.
2.2.2 Chlorin và các hợp chất chlorin
+ Đặc điểm;
Hypochlorit là chất khử khuẩn được sử dụng phổ biến nhất trong các cơ sở y tế. Loại hóa chất này tồn tại ở 2 dạng: dạng lỏng ( sodium hypochlorit hay Javen) hoặc dạng rắn (Calcium hypochlorit, sodium dichloroisocyanurat).
+ Cơ chế tác dụng:
Hợp chất chlorin làm ức chế phản ứng tạo ra enzyme cần thiết tham gia vào quá trình chuyển hóa trong tế bào vi khuẩn, làm thay đổi bản chất protein và bất hoạt các acid nucleic của vi khuẩn.
+ Cách sử dụng:
Dung dịch pha loãng từ 1/10 đến 1/100 của dung dịch sodium hypochlorite 5,25% được sử dụng để khử khuẩn các bề mặt thông thường ( sàn nhà, tương, trần nhà, mặt bàn xét nghiệm …). Nó còn được sử dụng giặt khử khuẩn đổ vải y tế, xử lý chất thải y tế, khử khuẩn các dụng cụ nha khoa, máy chạy thận nhân tạo. Chlorine được sử dụng phổ biến trong khử khuẩn nước.
Hoạt tính diệt khuẩn của dung dịch sodium hypochlorite bị giảm hoặc mất hoạt tính khi có mặt các chất hữu cơ, vì vậy cần được làm sạch trước khi khử khuẩn.
2.2.3 Formaldehyd
+ Đặc điểm:
Formaldehyd là chất khử khuẩn, tiệt khuẩn được sử dụng dưới hai dạng: dạng dung dịch và dạng khí. Chế phẩm được sử dụng phổ biến trong các cơ sở y tế là formalin, trong đó formaldehyd chiếm tỷ lệ 37% trọng lượng dung dịch. Dung dịch formaldehyd có tác dụng diệt khuẩn ( kể cả vi khuẩn lao), virus, nấm, bào tử.
Formaldehyd được xếp vào một trong các nhóm có khả năng gây ung thư cho những người tiếp xúc, vì vậy cần hạn chế tiếp xúc với loại hóa chất này.
+ Cơ chế tác dụng:
Formaldehyd bất hoạt vi sinh vật nhờ kiềm hóa nhóm amino, nhóm sulphydrat có trong phân tử protein và nguyên tử nitơ trong cấu trúc mạch vòng của gốc purin.
+ Cách sử dụng:
Formaldehyd là chất khử khuẩn, tiệt khuẩn mức độ cao, tuy nhiên nên hạn chế sử dụng vì:
- Có thể gây kích ứng da khi tiếp xúc.
- Là loại hóa chất có thể gây ung thư
- Có mùi khó chịu ngay cả khi ở nồng độ thấp
Trong các cơ sở y tế, formaldehyde được sử dụng chủ yếu vào các mục đích bất hoạt các chủng vacxin ( virus bại liệt, virus cúm) và bảo quản bệnh phẩm giải phẫu bệnh.
2.2.4 Glutaraldehyd
+ Đặc điểm:
Glutarldehyd là các dialdehyd bão hòa, được sử dụng như một chất khử khuẩn, tiệt khuẩn mức độ cao. Glutaraldehyd được sử dụng rộng rãi trong các cơ sở y tế vì:
- Hoạt tính diệt khuẩn tốt.
- Hoạt tính diệt khuẩn không bị thay đổi khi có mặt các chất hữu cơ ( đờm, máu, mủ).
- Không ăn mòn với các dụng cụ.
+ Cơ chế tác dụng:
Hoạt tính diệt khuẩn của glutaraldehyd được thực hiện nhờ khả năng kiềm hóa các nhóm sulfhydral, hydroxyl, carboxyl và amino của vi sinh vật, qua đó làm thay đổi cấu trúc ADN, ARN và quy trình tổng hợp protein của vi sinh vật.
+ Cách sử dụng:
Dung dịch glutaraldehyd 2% mang tính kiềm thường được sử dụng với mục đích khử khuẩn mức độ cao các dụng cụ kém chịu nhiệt như dụng cụ nội soi, dụng cụ gây mê, dụng cụ đo dung tích phổi và các dụng cụ khác sử dụng trong chẩn đoán, điều trị các bệnh đường hô hấp, các dụng cụ ngoại khoa thông thường bằng thép, nhôm, đồng.
Cách pha như sau: đổ lọ nhỏ đựng hóa chất vào can dung dịch Cidex và lắc kỹ, màu sắc sẽ thay đổi:
- Dung dịch cidex 145 ( 14 ngày) có màu xanh lá cây sau khi được hoạt hóa.
- Dung dịch cidex 285, 281 ( 28 ngày) có màu xanh dương sau khi được hoạt hóa.
- Dung dịch Posedex ( 14 ngày) có màu xanh sau khi hoạt hóa.
- Dung dịch Steranios ( 28 ngày) có màu xanh dương, không cần hoạt hóa.
2.2.5 Hydrogen peroxid
+ Đặc điểm:
Có hoạt tính diệt khuẩn tốt, có khả năng diệt vi khuẩn, virus, nấm và bào tử.
+ Cơ chế tác dụng:
Hydrogen peroxide phá hủy các gốc hydroxyl tự do, dẫn đến thay đổi cấu trúc màng lipid, ADN và thành phần thiết yếu khác của vi sinh vật
+ Cách sử dụng
Dung dịch hydrogen peroxid có tính ổn định cao, thường được sử dụng để khử khuẩn các bề mặt cố định ( máy đo nhãn áp, bóng thở). Nồng độ từ 6-25% có tác dụng tiệt khuẩn.
2.2.6 Hợp chất Iodophor
+ Đặc điểm:
Iodophor không có khả năng diệt bào tử nhưng có khả năng diệt vi khuẩn ( kể cả vi khuần lao), virus và nấm ở nồng độ khuyến cáo.
Chất khử khuẩn thuộc nhóm iodophor được sử dụng rộng rãi nhất trong các cơ sở y tế là povidone-iodin (kết hợp giữa ponivinylpyroiodin và iod). Chất này có ưu điểm là duy trì được hiệu quả diệt khuẩn của iod nhưng khác với iod là chúng không để lại màu sau khi sử dụng và ít gây kích ứng da hơn iod.
Hoạt tính diệt khuẩn của iodophor được thực hiện nhờ giải phóng cấc phân tử iode dạng tự do. Các hợp chất iodiphor khi được pha loãng có hiệu quả diệt khuẩn mạnh hơn so với hợp chất ban đầu. Điều này do các mối liên kết iodin trong chuỗi polimer bị suy yếu khi pha loãng dung dịch iodophor, vì thế làm tăng lượng iod tự do, dẫn đến tăng hiệu quả diệt khuẩn của dung dịch.
+ Cơ chế tác dụng:
Hợp chất iodophor có khả năng xâm nhập rất nhanh vào vách tế bào của vi sinh vật, phá vỡ cấu trúc protein và acid nucleic của vi sinh vật.
+ Cách dùng:
Các hóa chất thuộc nhóm iodophor được sử dụng trong sát khuẩn da và khử khuẩn các loại dụng cụ, vật dụng y tế như nhiệt kế, dụng cụ nội soi…
2.2.7 Orthopthaladehyde (OPA)
+ Đặc điểm:
OPA là loại hợp chất chứa 0,55% benzendicarboxylaldehyde, có khả năng diệt khuẩn tốt kể cả vi khuẩn lao.
+ Cơ chế tác dụng:
OPA là một chất khử khuẩn mới dược đưa vào sử dụng, cơ chế tác dụng vẫn chưa được xác định rõ.
+ Cách sử dụng:
Trên lâm sàng, OPA thường được sử dụng để khử khuẩn các dụng cụ nội soi. So với dung dịch glutraldehyde, OPA có tính ổn định cao hơn (hoạt tính diệt khẩn ổn định trong phạm vi pH thay đổi từ 3 – 9), không gây kích ứng da, không đòi hỏi phải hoạt hóa trước khi sử dụng. OPA có tác dụng diệt khuẩn nhanh ( 5 phút).
2.2.8 Paracetic acid
+ Đặc điểm:
Paracetic acid hay acid peroxyacetic là hợp chất có tác dụng diệt khuẩn nhanh, phổ kháng khuẩn rộng ( với hầu hết các loại vi khuẩn). Paracetic acid có khả năng diệt bào tử ở nhiệt độ thấp. Nó có thể ăn mòn một số loại dụng cụ: đồng, kẽm, thép. Dung dịch sau khi pha loãng không có tính ổn định cao ( dung dịch 1% giảm hiệu lực diệt khuẩn sau 6 ngày).
+ Cơ chế tác dụng:
Paracetic acid gây oxy hóa các liên kết sulfhydral và liên kết sulfua trong phân tử protein của vi sinh vật làm thay đổi cấu trúc phân tử protein của chúng.
+ Cách sử dụng:
Dung dịch paracetic acid nông độ 0,2% ở nhiệt độ 50°C có tác dụng tiệt khuẩn rất tốt, thường được sử dụng để tiệt khuẩn các dụng cụ ngoại khoa, nha khoa, dụng cụ nội soi. Chú ý tính ổn định của dung dịch này rất thấp ( thời hạn sử dụng không quá 24 giờ).
2.2.9 Phenolic
+ Đặc điểm:
Các loại hợp chất thuộc nhóm phenolic được tạo thành khi các nhóm chức như phenyl, alkyl, benzyl, halogen được thay thế 1 nguyên tử hydro trong cấu trúc vòng thơm. Hai chất thuộc nhóm phenol được sử dụng rộng rãi trong các qui trình khử khuẩn tại bệnh viện là orthophenylphenol và orthobenzyl- parochlorophenol. Hợp chất phenoic có khả năng diệt vi khuẩn ( kể cả vi khuẩn lao), virus, nấm
+ Cơ chế tác dụng:
Ở nồng độ cao, phenol xâm nhập vào tế bào và phá vỡ vách tế bào của vi sinh vật. Dung dịch phenol nồng độ thấp làm bất hoạt các enzym thiết yếu của vi sinh vật dẫn đến thiếu hụt các enzym tham gia vào quá trình chuyển hóa tại vách tế bào.
+ Cách dùng:
Được sử dụng rộng rãi trong bệnh viện với vai trò là chất tẩy rửa bề mặt trong phòng xét nghiệm, các dụng cụ, vật dụng y tế cần khử khuẩn thông thường.
2.2.10 Hợp chất Ammonium bậc 4
+ Đặc điểm:
Có khả năng diệt nấm, vi khuẩn, virus nhưng không có khả năng diệt bào tử.
+ Cơ chế tác dụng:
Các hợp chất ammonium bậc 4 làm bất hoạt các enzym sinh năng lượng, do vậy làm thay đổi bản chất các protein và làm phá vỡ màng tế bào vi sinh vật.
+ Cách sử dụng:
Được sử dụng rộng rãi để làm sạch bể mặt môi trường và các bể mặt chỉ cần khử khuẩn thông thường ( sàn nhà, tường, bể mặt các đồ dùng, vật dụng).
3. Các phương pháp tiệt khuẩn
Tiệt khuẩn là tiêu diệt mọi vi sinh vật. Về mặt hiệu lực, tiệt khuẩn được xác định khi lượng vi khuẩn chỉ còn một phần triệu.
Có hai phương pháp tiệt khuẩn: lý học và hóa học.
Tiệt khuẩn được áp dụng đối với mọi dụng cụ xâm nhập vào các tổ chức sống của cơ thể cũng như mọi loại thuốc và dịch truyền.
Mọi dụng cụ cần được đóng gói trước khi tiệt khuẩn. Các dụng cụ đã được tiệt khuẩn chỉ được coi là vô khuẩn khi được để trong một gói kín, nguyên vẹn.
3.1 Tiệt khuẩn bằng nhiệt:
* Tiệt khuẩn bằng hơi nước (nhiệt ướt): tiếp xúc với hơi nước bão hòa ở nhiệt độ 121°C trong 30 phút hoặc 134°C trong 13 phút.
- Ưu điểm: thời gian tiệt khuẩn ngắn, không độc, không tốn kém.
- Nhược điểm: làm hư hại các bộ phận nhậy cảm với nóng và ẩm.
* Tiệt khuẩn bằng hơi nóng khô: tiếp xúc ở nhiệt độ 160°C trong 120 phút hoặc 170°C trong 60 phút. Phương pháp này kém hiệu quả hơn phương pháp tiệt khuẩn bằng nhiệt ướt, đặc biệt đối với các dụng cụ có lòng ống hẹp.
- Ưu điểm: Độ ăn mòn thấp, an toàn cho môi trường.
- Nhược điểm: thời gian tiệt khuẩn dài.
3.2 Tiệt khuẩn bằng hóa chất:
* Ethylen oxid (EO):
– Ưu điểm:
- Xuyên qua vật liệu đóng gói và nhiều loại nhựa.
- Thích hợp với hầu hết vật liệu y tế.
- Giám sát và vận hành đơn giản.
– Nhược điểm:
- Cần thời gian thông khí, chu kỳ tiệt khuẩn dài (2-5 giờ).
- EO là chất độc có khả năng gây ung thư và dễ cháy.
* Tiệt khuẩn bằng Hydrogen peroxid:
– Ưu điểm:
- Thích hợp với dụng cụ nhạy cảm với nhiệt.
- An toàn cho môi trường và nhân viên.
- Không có chất cặn độc hại.
- Vận hành và giám sát đơn giản.
– Nhược điểm:
- Không thể tiệt khuẩn cellulose, đồ vải và chất lỏng.
- Không tiệt khuẩn được với những vật dụng y tế dài, lòng ống hẹp.
- Cần đóng gói giấy tổng hợp.
* Formaldehyd:
Ưu điểm:
- Không gây cháy nổ.
- Thích hợp với hầu hết vật liệu y tế.
Nhược điểm:
- Là hóa chất độc và gây dị ứng
- Cần thời gian tiệt khuẩn dài.
4. Giám sát qui trình tiệt khuẩn:
Có ba phương pháp khác nhau để giám sát qui trình tiệt khuẩn: cơ học, hóa học và sinh học. Giám sát cơ học và hóa học chỉ cung cấp các chỉ thị để đạt được sự tiệt khuẩn có thể nhìn thấy được, như thời gian, nhiệt độ và áp xuất. Chỉ có chỉ thị sinh học mới cho biết hiệu quả thực sự của qui trình tiệt khuẩn, là nhằm diệt tất cả vi khuẩn, bao gồm cả các bào tử.
- Cơ học: biểu đồ, đồ thị thời gian và nhiệt độ.
- Hóa học: dây thử, giấy thử hay viên thuốc thử nhạy cảm với nhiệt độ hay độ ẩm.
- Sinh học: Test sinh học ( hàng tuần hoặc hàng tháng và sau mỗi lần sữa chữa máy). Với tiệt khuẩn bằng nhiệt ướt (autoclave) sử dụng loại Bacillus stearothermophilus, với EO sử dụng loại Bacillus subtilis
Vô cảm cho bệnh nhân nội soi ổ bụng
1. LỊCH SỬ CỦA PHẪU THUẬT NỘI SOI HIỆN ĐẠI
Trường hợp sử dụng nội soi ổ bụng chẩn đoán lâm sàng trên người đầu tiên được thực hiện bởi H.Jacobaeus vào năm 1910. Cho tới thập kỷ 70 do có sự cải tiến về công nghệ và an toàn thiết bị cho nên phẫu thuật nội soi phụ khoa qua đường ổ bụng được thực hiện thường quy hơn. Lần đầu tiên vào năm 1983 tác giả Semm đã thực hiện phẫu thuật cắt ruột thừa nội soi, và vào năm 1985 tác giả Muhe đã thực hiện phẫu thuật cắt túi mật nội soi. Từ đó phẫu thuật nội soi đã nhanh chóng phát triển và mở rộng bao gồm nhiều loại phẫu thuật khác nhau.
2. DANH SÁCH MỘT SỐ PHẪU THUẬT NỘI SOI Ổ BỤNG THƯỜNG ĐƯỢC THỰC HIỆN NGÀY NAY
- 2.1 Phẫu thuật phụ khoa: cắt tử cung qua đường âm đạo, thắt ống dẫn trứng, soi tử cung, cắt bỏ buồng trứng, tạo hình vòi trứng
- 2.2. Phẫu thuật dạ dày ruột: ruột thừa, đại tràng, ruột non, túi mật và ống mật chủ, dạ dày, thực quản, gan, lách, tụy, tuyến thượng thận, sửa chữa thoát vị, nội soi ổ bụng chẩn đoán, gỡ dính
3. LỢI ÍCH CỦA PHẪU THUẬT NỘI SOI SO VỚI PHẪU THUẬT MỞ
- 3.1. Lợi ích trong phẫu thuật: Đáp ứng với stress giảm với giảm các chất phản ứng giai đoạn cấp (protein C phản ứng và interleukin-6), giảm đáp ứng chuyển hóa với giảm tăng đường máu và tăng bạch cầu, giảm dịch chuyển dịch thể, chức năng miễn dịch hệ thống được bảo tồn tốt hơn, và tránh được phơi bày các tạng trong ổ bụng
- 3.2. Lợi ích sau phẫu thuật: Đau sau phẫu thuật ít hơn, giảm nhu cầu thuốc giảm đau, cải thiện chức năng hô hấp do bởi đau ít hơn, giảm xẹp phổi, vận động sớm hơn, cải thiện thẩm mỹ do đường rạch nhỏ hơn, nhiễm trùng vết mổ ít hơn, giảm tắc ruột sau phẫu thuật, giảm thời gian nằm viện
4. VÔ CẢM TRONG PHẪU THUẬT NỘI SOI Ổ BỤNG
4. 1. Chống chỉ định của phẫu thuật nội soi ổ bụng
- Bệnh tim mạch: bệnh tim bẩm sinh, bệnh van tim, xơ vữa động mạch, bệnh mạch vành, cao huyết áp không được điều trị đã có biến chứng ở não, tim, thận. Bệnh nhân sốc chấn thương, sốc mất máu.
- Bệnh lý phổi: bệnh phổi mãn tính, khí phế thũng, hen phế quản, kén khí phổi
- Bệnh lý thần kinh: tăng áp lực nội sọ, tăng nhãn áp, di chứng của chấn thương sọ não hoặc đang theo dõi chấn thương sọ não
- Các chống chỉ định khác: bệnh lý đông máu, bệnh nhân có mổ cũ ổ bụng, suy thận
4.2. Ảnh hưởng tư thế trong mổ nội soi ổ bụng đến các cơ quan
4.2.1. Tư thế Trendelenburg (đầu thấp):
- Cung lượng tim và áp lực tĩnh mạch trung tâm tăng và bệnh nhân với phản xạ thụ thể áp lực nguyên vẹn sẽ xảy ra giãn mạch và nhịp tim chậm. Tư thế này có lẽ giảm mất máu nhưng gia tăng nguy cơ tắc mạch khí
- Các ảnh hưởng trên phổi bao gồm suy giảm chức năng cơ hoành thứ phát do bởi dịch chuyển về phía đầu của các tạng trong ổ bụng, dẫn đến giảm dung tích cặn chức năng, giảm dung tích phổi toàn bộ, giảm compliance phổi, dẫn đến xẹp phổi phát triển. Dịch chuyển của phổi và cựa khí quản (carina) về phía đầu có thể làm cho ống nội khí quản đi sâu vào phế quản.
4.2.2. Tư thế Trendelenburg đảo ngược (đầu thấp):
- Giảm tiền gánh, dẫn đến giảm cung lượng tim và huyết áp động mạch trung bình. Máu sẽ đọng ở chi dưới có thể dẫn đến gia tăng nguy cơ huyết khối tĩnh mạch và tắc mạch phổi.
- Chức năng phổi được cải thiện.
4.3. Ảnh hưởng của bơm CO2 đến các cơ quan
- Việc lựa chọn khí bơm tạo khoang ổ bụng bị ảnh hưởng bởi độ hòa tan khí máu, tính thấm của tạng, khả năng cháy nổ, giá thành và khả năng gây ra các tác dụng phụ. Khí lý tưởng phải là khí trơ, không màu, có khả năng đào thải qua phổi. Mặc dù có một số khí đã được sử dụng nhưng CO2 vẫn là khí được lựa chọn thông dụng hơn cả.
- Khi bơm CO2 gây tăng PaCO2. Mức độ tăng PaCO2 lệ thuộc vào áp lực trong ổ bụng, tuổi bệnh nhân và tình trạng bệnh tật, tư thế bệnh nhân và phương thức thông khí. Trên bệnh nhân khỏe mạnh, cơ chế chủ yếu của việc gia tăng PaCO2 là hấp thụ qua phúc mạc. Ngoài ra, tăng áp lực ổ bụng dẫn đến rối loạn chức năng cơ hoành và tăng khoảng chết phế nang, dẫn đến giảm thông khí và hậu quả gia tăng PaCO2. PaCO2 tăng khoảng 5-10 phút sau bơm CO2 và thường đạt mức bình nguyên sau 20-25 phút.
- Khuyến cáo hiện tại cho áp lực trong ổ bụng khi phẫu thuật nội soi ổ bụng là nhỏ hơn 15 mmHg và phần lớn các phẫu thuật nội soi được thực hiện với áp lực này trong phạm vi 12-15 mmHg. Nói chung, áp lực này nhỏ hơn 10 mmHg có ảnh hưởng sinh lý tối thiểu. Áp lực bơm trên 16 mmHg dẫn đến các thay đổi sinh lý không mong muốn như là giảm cung lượng tim, tăng sức cản mạch toàn thể, tăng trở kháng cơ học của phổi và thành ngực. Với áp lực trên 20 mmHg, dòng máu thận, tốc độ lọc cầu thận, cung lượng nước tiểu giảm. Áp lực thấp 7 mmHg và nội soi không bơm khí được ủng hộ như là một biện pháp giảm mức độ xáo trộn huyết động kết hợp với áp lực cao.
4.3.1. Ảnh hưởng trên huyết động: những thay đổi được nhận thấy trong cung lượng tim là hai giai đoạn: ban đầu giảm cung lượng tim khi khởi mê và bắt đầu bơm CO2; trong 5-10 phút, cung lượng tim bắt đầu tăng, tiếp cận tới giá trị trước bơm. Với áp lực trong ổ bụng trên 10 mmHg, giảm máu tĩnh mạch trở về nhưng áp lực làm đầy tim tăng với bơm CO2 chủ yếu do bởi tăng áp lực trong lồng ngực. Sức cản mạch máu toàn thể và huyết áp trung bình cũng tăng đáng kể trong giai đoạn đầu bơm khí. Mặc dù những thay đổi này sẽ hồi phục một phần khoảng 10-15 phút sau bơm khí, nhưng những thay đổi ở áp lực làm đầy tim và sức cản mạch hệ thống gây tăng stress thành thất trái.
4.3.2. Thay đổi hô hấp: việc bơm CO2 kèm theo gia tăng áp lực trong ổ bụng dẫn đến dịch chuyển cơ hoành về phía đầu, giảm dung tích cặn chức năng và compliance. Tư thế Trendelenburg làm nặng thêm những thay đổi này. Khi dung tích cặn chức năng giảm liên quan tới dung tích đóng của bệnh nhân, thiếu oxy máu có lẽ do bởi xẹp phổi và shunt trong phổi. Thiếu oxy máu không thường gặp ở bệnh nhân khỏe mạnh nhưng liên quan tới bệnh nhân béo bệu hoặc bệnh lý tim phổi
4.3.3. Đáp ứng thần kinh thể dịch: nồng độ huyết tương của dopamin, vasopressin, epinephrin, norepinephrin, renin, angiotensin và cortisol tăng đáng kể. Việc gia tăng này tương ứng với khi bắt đầu bơm khí. Mức huyết thanh của vasopressin và norepinephrin liên quan chặt chẽ với những thay đổi được nhận thấy ở cung lượng tim, huyết áp động mạch trung bình và sức cản mạch toàn thể. Ưu thán, những ảnh hưởng cơ học của bơm khí và kích thích hệ thần kinh tự động được cho là các nguyên nhân của những thay đổi trên. Việc sử dụng trước mổ các thuốc chủ vận alpha2 như clonidin hoặc dexmedetomidin cho thấy giảm đáp ứng stress.
4.4. Chọn lựa phương pháp vô cảm trong phẫu thuật nội soi ổ bụng
Gây tê tại chỗ kèm an thần tĩnh mạch, gây tê vùng, gây mê toàn thân có thể được sử dụng. Việc chuyển từ phẫu thuật nội soi sang phẫu thuật mở phải được dự tính khi lựa chọn phương pháp vô cảm
4.4.1. Gây tê tại chỗ kèm an thần tĩnh mạch:
- Thuận lợi bao gồm rút ngắn thời gian vô cảm, hồi phục nhanh hơn, giảm biến chứng buồn nôn và nôn sau mổ, phát hiện sớm các biến chứng, và ít biến đổi huyết động hơn.
- Thành công phụ thuộc vào sự cộng tác của bệnh nhân, kỹ thuật phẫu thuật chính xác, và thời gian phẫu thuật ngắn.
- Tránh sử dụng phương pháp vô cảm này cho các phẫu thuật kéo dài yêu cầu đặt nhiều vị trí trocar, tư thế dốc, và tăng nhiều áp lực trong ổ bụng.
4.4.2. Gây tê vùng:
Thuận lợi và bất lợi tương tự gây tê tại chỗ. Tuy nhiên việc hủy thần kinh giao cảm mức cao phối hợp với bơm khí ổ bụng và tư thế có thể kết hợp với những thay đổi bất lợi về hô hấp và tuần hoàn.
4.4.3. Gây mê toàn thân: đặt nội khí quản thông khí nhân tạo vòng kín có vôi Sôđa là phương pháp vô cảm thường sử dụng nhất.
- Thuận lợi bao gồm giãn cơ tối ưu, giảm đau hoàn toàn, có khả năng kiểm soát hô hấp, phòng ngừa trào ngược và trường mổ yên tĩnh.
- Tiền mê nên phối hợp giữa thuốc an thần như seduxen hoặc hypnoven và thuốc đối kháng tác dụng tăng tiết của hệ thần kinh thực vật như atropin để giảm tối đa những phản xạ do tác động của áp lực bơm hơi ổ bụng.
- Khởi mê và duy trì mê phải đủ sâu tránh để bệnh nhân thở lại trong lúc bơm hơi. Dùng các thuốc mê ít ức chế cơ tim, ít kích thích hệ thống thần kinh thực vật như propofol, isofluran, sevofluran.
- Thuốc giảm đau trung ưong dòng họ morphin như fentanyl, sufentanil.
- Thuốc giãn cơ nên dùng loại giãn cơ không khử cực có thời gian tác dụng trung bình như norcuron, esmeron.
- Cài đặt ban đầu các thông số trên máy thở: thể tích khí lưu thông (Vt) = 8-10 mL/kg và tần số (f) = 10 – 12 lần/phút
- Cài đặt các thông số cho máy bơm CO2: đặt giới hạn an toàn áp lực 10-12 mmHg, lưu lượng khí bơm ban đầu 2-2,5 lít/phút
- Giai đoạn thoát mê phải để bệnh nhân tỉnh hẳn, tự thở tốt, dùng thuốc giải giãn cơ hệ thống trước khi rút ống nội khí quản.
4.5. Các biến chứng kết hợp với phẫu thuật nội soi ổ bụng và bơm CO2
Các biến chứng thường xảy ra khi đặt trocar qua thành bụng và trong khi bơm CO2
- Các biến chứng trong mổ: tổn thương mạch máu lớn, chảy máu, đâm thủng tạng, tổn thương bàng quang niệu quản, bỏng, rối loạn nhịp tim (phân ly nhĩ thất, nhịp nút, nhịp tim chậm, và vô tâm thu), ưu thán, thiếu oxy máu, tràn khí CO2 dưới da, tràn khí màng phổi, nghẽn mạch khí, đặt ống nội khí quản vào phế quản, tăng áp lực nội sọ, trào ngược, tổn thương thần kinh ngoại vi.
- Các biến chứng sau mổ: buồn nôn và nôn, đau, kích thích vai và cổ, huyết khối tĩnh mạch sâu, chảy máu muộn, viêm phúc mạc, nhiễm trùng vết mổ, rối loạn chức năng hô hấp, thoát vị vết mổ, và di căn khối u
Vô cảm cho mổ u tủy thượng thận
1. ĐẠI CƯƠNG
U tủy thượng thận là các khối u tiết catecholmin bắt nguồn từ các tế bào ưa chrom trong tủy thượng thận. U tủy thượng thận chiếm khoảng 0,1 % tổng số các trường hợp tăng huyết áp ở người lớn. Mặc dù nó là nguyên nhân gây tăng huyết áp không phổ biến nhưng việc chẩn đoán có hay không có u tủy thượng thận ở bệnh nhân tăng huyết áp là điều bắt buộc vì nguy cơ tử vong cao và đó là một trong những thể tăng huyết áp có thể điều trị được thực sự. Tăng tiết catecholamin không kiểm soát có thể gây tăng huyết áp ác tính, tai biến mạch máu não và nhồi máu cơ tim. Đó là những thách thức lớn cho bác sĩ gây mê cả trong phòng mổ cũng như tại đơn vị chăm sóc tích cực sau mổ. Trước những năm 1960, chưa có xét nghiệm sàng lọc nước tiểu và sử dụng các thuốc ức chế anpha adrenergic điều trị trước mổ, có khoảng 25 % đến 50% bệnh nhân (nội trú có u tủy thượng thận) tử vong khi khởi mê hoặc các rối loạn không liên quan trong khi mổ.
Nguyên nhân chính xác của u tủy thượng thận vẫn còn chưa rõ ràng. Khoảng 90% các trường hợp u tủy thượng thận được phát hiện mang tính chất tự phát, 10% mang tính chất di truyền gia đình khi có tính trạng trội của nhiễm sắc thể thường. Hai giới có tỷ lệ mắc như nhau, u tủy thượng thận có thể gặp ở bất kỳ lứa tuổi nào nhưng thường gặp nhất ở độ tuổi 30 đến 50. Ở trẻ em, tỷ lệ mắc khoảng 10%, các triệu chứng lâm sàng thường không đặc hiệu nên rất khó chẩn đoán. Các u tuyến thượng thận mang tính chất gia đình thường gặp là u tuyến ở cả hai bên hoặc các khối u ở ngoài tuyến thượng thận nhưng cùng vị trí giải phẫu xuất hiện ở các thế hệ kế tiếp trong gia đình. Những tiến bộ gần đây cho phép chẩn đoán sớm u tủy thượng thận mang tính chất gia đình trước khi xuất hiện các triệu chứng lâm sàng nhờ chẩn đoán gen. U tủy thượng thận gia đình có thể là một phần của hội chứng u nhiều tuyến nội tiết và có liên quan tới loạn sản tế bào ngoại bì thần kinh. Các bệnh nhân có hội chứng u nhiều tuyến nội tiết nhóm 2a có u tủy thượng thận, ung thư nhân tuyến giáp và cường tuyến cận giáp. Các bệnh nhân nhóm 2b có u tủy thượng thận, ung thư nhân tuyến giáp, các u hạch thần kinh đường tiêu hóa, dày thần kinh giác mạc, hội chứng marfan. Thường gặp u tủy thượng thận cả hai bên cơ thể và rất hiếm khi ác tính ở các bệnh nhân có hội chứng u nhiều tuyến nội tiết 2a và 2b. Gần như 100% bệnh nhân ở cả hai nhóm 2a và 2b có hoặc sẽ phát triển thành u tủy thượng thận lành tính 2 bên, loạn sản bì thần kinh. Khoảng 10% đến 25% bệnh nhân mắc hội chứng Von Hippel-Lindau (u mạch ở tiểu não và võng mạc) có thể có u tủy thượng thận; khoảng 1% bệnh nhân mắc bệnh Recklinghausen (u xơ thần kinh) có u tủy thượng thận, các bệnh nhân có xơ cứng rễ và hội chứng Sturge-Weber có u tủy thượng thận.
U ác tính tuyến thượng thận có thể di căn qua đường tĩnh mạch tới các cơ quan chiếm ưu thế như gan và xương, mặc dù tủy sống, phổi não và các hạch bạch huyết cũng có thể bị. Nhìn đại thể bề ngoài các khối di căn như một khối u lành tính. Tỷ lệ ác tính khoảng 10%, tỷ lệ này có thể tăng cao do ngày càng tiến bộ trong các phương tiện chẩn đoán trong tương lai. Tỷ lệ sống trên 5 năm với u ác tính tủy thượng thận là 44%, khoảng 5% – 10% có tái phát sau khi cắt u tủy thượng thận lành tính.
Khoảng 80% các khối u tủy thượng thận khu trú ở tủy thượng thận, bên phải thường bị nhiều hơn bên trái. Khoảng 20% u tuyến thượng thận khu trú ở ngoài tuyến thượng thận (lạc chỗ), chủ yếu là trong ổ bụng và liên quan tới hạch giao cảm. Các vị trí giải phẫu gần chỗ chia nhánh của động mạch chủ là vị trí thường gặp nhất của u tuyến thượng thận lạc chỗ, khoảng 2% lạc chỗ lên ngực và cổ. Khoảng 10% các u tủy thượng thận gặp ở trẻ em, trong đó có 30 % bệnh nhân có nhiều khối u, 30% có khối u lạc chỗ, 20% có u thượng thận hai bên và gặp ở trẻ em nhiều hơn người lớn.
Sự phát triển của u tuyến thượng thận lạc chỗ được giải thích do không có khả năng teo nhỏ các mô ưa chrome ở thời thơ ấu. Trái ngược với sự hiểu biết trước đây, hầu hết các u tủy thượng thận lạc chỗ có quá trình tiến triển lành tính. Các u tuyến thượng thận ở người trưởng thành có đặc điểm là khối đặc, giàu mạch máu, đường kính từ 3-5 cm, trọng lượng trung bình 100 g (dao động từ 1 – 4000 g). Các khối u có kích thước lớn ở người trưởng thành có thể chứa từ 100-800 mg norepinephrin.
Các u tủy thượng thận là các u của hệ thần kinh giao cảm. Hệ thần kinh giao cảm còn nguyên vẹn và hoạt động cùng sự hiện diện của khối u. Các biểu hiện lâm sàng của u tủy thượng thận là kết quả giải phóng hormon của khối u. Hầu hết các khối u tủy thượng thận tiết ra mình norepinephrin, hoặc phổ biến hơn là tiết cùng một lượng nhỏ epinephrin với tỉ lệ 85:15, tuyến thượng thận bình thường tiết ra hormon với tỉ lệ đảo ngược (15:85). Có khoảng 15% khối u tiết epinephrin nhiều hơn, một số tiết ra cả dopamin. Hầu hết các u tủy thượng thận tiết catecholamin một cách tự động mà không bị kiểm soát bởi hệ thần kinh.
2. TRIỆU CHỨNG LÂM SÀNG
Tăng huyết áp liên tục hoặc kịch phát là biểu hiện thường xuyên nhất của u tuyến thượng thận. Các triệu chứng kinh điển gồm đau đầu, vã mồ hôi, xanh sao và đánh trống ngực. Hầu hết bệnh nhân có các triệu chứng và sự bùng phát, phạm vi thay đổi từ không thường xuyên (một lần một tháng hoặc ít hơn) cho đến dữ dội (nhiều lần một ngày), có thể kéo dài từ vài phút đến vài giờ. Các triệu chứng có thể tự phát hoặc được thúc đẩy khi tăng hoạt động thể lực hoặc kích thích tâm lý hoặc các thuốc. Tăng huyết áp gặp ở trên 80% bệnh nhân trưởng thành. Tăng huyết áp kịch phát xen giữa các giá trị huyết áp bình thường xảy ra ở khoảng 50% bệnh nhân, khoảng 30% bệnh nhân có biểu hiện tăng huyết áp liên tục. Theo dõi huyết áp liên tục 24 giờ trên monitor cho thấy nhiều cơn tăng huyết áp mà không có triệu chứng. Hạ huyết áp tư thế cũng là một dấu hiệu thường gặp và được coi là giảm thể tích tuần hoàn thứ phát do giảm đáp ứng với phản xạ co động, tĩnh mạch với các chất co mạch. Các dấu hiệu về huyết động tùy thuộc vào loại catecholamin nào tiết ra chiếm ưu thế. Khi norepinephrin được tiết ra nhiều hơn, tác dụng anpha-adrenergic mạnh hơn nên bệnh nhân có biểu hiện tăng huyết áp tâm thu và tâm trương cùng với phản xạ chậm nhịp tim. Khi u tuyến thượng thận tiết nhiều epinephrin hơn, tác dụng beta-adrenergic là chủ yếu nên có biểu hiện tăng huyết áp tâm thu, hạ huyết áp tâm trương và nhịp tim nhanh. Một số bệnh nhân có huyết áp bình thường mặc dù có mức norepinephrin cao trong hệ tuần hoàn. Ở bệnh nhân u tủy thượng thận việc điều chỉnh huyết áp động mạch phức tạp hơn các quan điểm truyền thống. Mức tăng huyết áp động mạch dường như có ít liên quan với mức catecholamin đang lưu hành trong hệ tuần hoàn. Nguyên nhân có thể do sự mất cân bằng giữa các chất giãn mạch nội sinh (như dopamin, serotonin, enkephalin và các chất vận mạch ở ruột) và các catecholamin trong hệ tuần hoàn. Mặc dù mức catecholamin trong hệ tuần hoàn có thể cao hơn gấp hàng chục lần ở các bệnh nhân u tủy thượng thận nhưng sự biến đổi huyết động không có khác biệt đáng kể so với các bệnh nhân cao huyết áp nguyên phát. Cả hai loại này đều có tăng sức kháng thành mạch, cung lượng tim vẫn bình thường, nhưng có giảm nhẹ thể tích huyết tương. Sự tăng cao của catecholamin trong huyết tương lâu dài không gây ra đặc điểm đặc trưng trong đáp ứng huyết động cấp tính. Điều này có thể do giảm sự nhạy cảm của hệ tim mạch hoặc giảm sự điều hòa các receptor adrenergic. Giảm sự nhạy cảm thứ phát của các tế bào cơ trơn do giảm số lượng các receptor hoặc thay đổi ở khớp nối thần kinh cơ. Tuy nhiên, sự đáp ứng huyết động của các cơn tăng huyết áp xảy ra tương tự như tăng cấp tính catecholamin. Mạch máu của các bệnh nhân u tủy thượng thận thường cần một nồng độ catecholamin rất cao mới có đáp ứng co mạch tăng huyết áp.
Bệnh cơ tim có thể làm giảm đáp ứng của tim với catecholamin. Tác động thực sự của bệnh cơ tim tới các triệu chứng lâm sàng còn chưa rõ ràng. Giảm toàn bộ chức năng bơm của cơ tim do giảm mạng lưới các nguyên bào trong cơ tim và giảm sự điều hòa của các receptor beta. Nguyên nhân do nhiều yếu tố gây ra bao gồm thay đổi giảm tính thấm của catecholamin qua màng tế bào dẫn tới tăng ồ ạt ion calci, nhiễm độc các sản phẩm oxi hóa catecholamin, gây nguy hại cho các gốc tự do. Hơn nữa, nồng độ catecholamin cao ảnh hưởng lên tim thông qua sự co động mạch vành vì tác động lên receptor anpha-adrenergic, gây giảm dòng máu vành và nguy cơ thiếu máu cơ tim. Cả bệnh cơ tim thể giãn và phì đại cơ tim cũng như tắc nghẽn dòng máu về tim trái đã được đánh giá qua siêu âm tim. Kết quả cho thấy siêu âm tim bình thường ở những bệnh nhân không có các triệu chứng ở hệ tim mạch (khó thở, đau ngực) hoặc các dấu hiệu lâm sàng khác có liên quan đến tim. Điện tim bất thường có thể gồm sự chênh lênh hoặc lõm xuống của đoạn ST, sóng T đảo ngược hoặc nằm ngang, kéo dài khoảng QT, sóng P cao, trục chuyển trái và rối loạn nhịp. Những sự thay đổi này mang tính thoáng qua, có thể thay đổi và trở lại bình thường với các thuốc ức chế anpha và hoặc thuốc ức chế beta. Bệnh cơ tim có thể được hồi phục nếu loại bỏ được các kích thích catecholamin trước khi xảy ra xơ hóa các nguyên bào sợi cơ tim. Khác với bệnh cơ tim, các bệnh u tủy thượng thận có thể dẫn tới suy tim xung huyết có phì đại cơ tim thứ phát do tăng huyết áp liên tục. Vì các u tủy thượng thận có sự thay đổi rõ ràng trong hoạt động bài tiết hormon, có thể nhầm lẫn với nhiễm độc giáp, tăng huyết áp ác tính, đái đường, hội chứng ung thư hạch hoặc nhiễm khuẩn gram âm. Các bệnh nhân u tủy thượng thận hiếm khi có mức đường máu bình thường, hầu hết đều tăng đường máu thứ phát do catecholamin kích thích tổng hợp phân giải glycogen và ức chế bài tiết insulin.
3. CHẨN ĐOÁN
Khi lâm sàng có nghi ngờ u tủy thượng thận cần làm định lượng catecholamin. Có nhiều các xét nghiệm được sử dụng để chẩn đoán u tủy thượng thận nhưng không có xét nghiệm nào là lý tưởng. Dù có lựa chọn làm xét nghiệm nào chăng nữa cũng cần kiểm soát chặt chẽ các tình huống trong lâm sàng (như tập thể dục, sự xúc động, sử dụng các thuốc) để có kết quả đáng tin cậy. Một số yếu tố như uống rượu, nhược giáp, giảm thể tích máu… có thể làm sai lệch các kết quả xét nghiệm chẩn đoán u tủy thượng thận.
Xét nghiệm nhạy cảm nhất cho các bệnh nhân có nguy cơ cao (u tủy thượng thận gia đình hoặc có các triệu chứng điển hình) là định lượng các chất chuyển hóa tự do của catecholamin trong huyết tương. Các catecholamin bị chuyển hóa thành các chất chuyển hóa tự do trong các tế bào của khối u, các chất chuyển hóa này được phóng thích liên tục vào hệ tuần hoàn. Chẩn đoán u tủy thượng thận khi xét nghiệm normetanephrine lớn hơn 400 pg/mL và hoặc metanephrine lớn hơn 220 pg/mL trong huyết tương. Nghi ngờ chẩn đoán nếu giá trị của normetanephrine từ 112 -400 pg/mL hoặc metanephrine từ 61 – 220 pg/mL. Loại trừ u tủy thượng thận nếu normetanephrine thấp hơn 112 pg/mL và metanephrine thấp hiwn 61 pg/mL.
Xét nghiệm catecholamin tự do trong nước tiểu và các chất chuyển hóa của nó (như metanephrine, normetanephrine, acid vanillylmandelic) cũng thường được sử dụng để chẩn đoán u tủy thượng thận. Xét nghiệm rất dễ thực hiện và có sẵn, tuy nhiên việc thu thập nước tiểu 24 giờ không tiện lợi và không đáng tin cậy. Định lượng acid vanillylmandelic (chất chuyển hóa cuối cùng của catecholamin) là xét nghiệm rẻ và kinh điển nhất nhưng không đặc hiệu. Xác định mức tăng cao của metanephrin là xét nghiệm nước tiểu tốt nhất. Với những bệnh nhân ít có khả năng bị u tủy thượng thận, chỉ cần xét nghiệm định lượng metanephrine và catecholamines nước tiểu 24 giờ là đủ.
Định lượng chính xác nồng độ catecholamin huyết tương là xét nghiệm đầu tiên được chỉ định. Một số lượng lớn bệnh nhân có tăng đáng kể norepinephrin, epinephrin hoặc cả hai, mặc dù một vài bệnh nhân u tủy thượng thận có nồng độ catecholamin bình thường lúc nghỉ. Chẩn đoán xác định u tủy thượng thận khi tổng nồng độ catecholamin huyết tương lớn hơn 2000 pg/mL. Nghi ngờ khi giá trị tổng lượng catecholamin nằm trong khoảng từ 500 đến 2000 pg/mL và loại trừ khi giá trị thấp hơn 500 pg/mL. Trong phần lớn các trường hợp, sự tăng cao catecholamin ở cả huyết tương hoặc catecholamin tự do và các chất chuyển hóa của nó trong nước tiểu đủ thỏa mãn để chẩn đoán xác định. Kết quả không rõ ràng trong 5-10% số bệnh nhân và trong những trường hợp này, sử dụng test “ngăn chặn” bằng clonidin. Clonidin là thuốc ức chế anpha 2 tác động trên hệ thống thần kinh trung ương để giảm bớt hoạt động của giao cảm ly tâm. Ở những bệnh nhân u tủy thượng thận, nồng độ catecholamin tăng trong huyết tương do khối u tăng tiết, bỏ qua cơ chế tiết và lưu giữ bình thường. Clonidin tác dụng làm giảm catecholamin huyết tương ở những bệnh nhân không có u tủy thượng thận trong khi không có tác dụng hạ catecholamin ở bệnh nhân u tủy thượng thận.
Trước đây, sử dụng test kích thích tăng tiết catecholamin từ khối u bằng histamin và tyramin. Tuy nhiên, điều này làm tăng tỷ lệ biến chứng và tử vong nên hiện nay đã bị cấm sử dụng. Test kích thích bằng glucagon hiện nay được coi là an toàn nhất và là test kích thích đặc hiệu nhất. Glucagon tác động trực tiếp lên khối u để giải phóng catecholamin. Xét nghiệm này ở những bệnh nhân có huyết áp tâm thu thấp hơn 100 mmHg. Test được coi là dương tính nếu catecholamin huyết tương tăng ít nhất ba lần so với giá trị ban đầu hoặc tăng cao hơn 2000 pg/mL trong vòng từ 1-3 phút tiêm glucagon. Hiện nay, hầu hết các trung tâm chẩn đoán u tủy thượng thận bằng xét nghiệm nước tiểu định lượng catecholamin tự do và chất chuyển hóa của nó hoặc xét nghiệm mức catecholamin huyết tương, sử dụng test clonidin hoặc test kích thích bằng glucagon ở những trường hợp nghi ngờ. Trong số các test này, xét nghiệm nào là đáng tin cậy nhất vẫn còn đang gây tranh cãi.
Vị trí khối u có thể được dự đoán dựa vào tính chất catecholamin tiết ra (bảng 1). Các xét nghiệm chẩn đoán hình ảnh chuyên biệt có thể cho biết vị trí chính xác khối u. Chụp cắt lớp vi tính (CT) và cộng hưởng từ (MRI) là các phương pháp chẩn đoán không xâm lấn tối ưu cho phép xác định vị trí giải phẫu của u tủy thượng thận. CT xác định được trên 95% các khối u tủy thượng thận có đường kính lớn hơn 1cm. MRI có nhiều ưu điểm hơn CT vì phân biệt được các tổn thương nhỏ hơn của tuyến thượng thận, phân biệt tốt hơn các tổn thương khác nhau của tuyến thượng thận, không cần dùng chất cản quang tĩnh mạch, không bị phơi nhiễm với tia xạ. Trên chuỗi hình ảnh MRI, u tủy thượng thận có cường độ tín hiệu cao và tăng sáng. CT và MRI cung cấp các thông tin chủ yếu về mặt giải phẫu, ngược lại xạ hình ký bằng meta-iodobenzylguanidin đánh dấu bằng iod 131 và iod 123 (131I-MIBG và 123I-MIBG) lại cung cấp nhiều thông tin về mặt chức năng. MIBG là đồng phân của guanethidin, có cấu trúc tương tự norepinephrin, bị bắt giữ ở các neuron adrenergic và tập trung ở các khối u tiết catecholamin. MIBG được xác định qua xạ hình. Đây là một xét nghiệm mang tính chất sinh lý học qua đó để xác định vị trí khối u thượng thận dựa trên hoạt động dược lý học. Nó rất có hiệu quả trong việc xác định các khối u tủy thượng thận lạc vị trí, các khối di căn và khẳng định khối thượng thận có chức năng của u tủy thượng thận. MIBG cho phép quan sát toàn bộ cơ thể và là lựa chọn hàng đầu để xác định vị trí khối u tủy thượng thận. CT, MRI và xạ hình ký 131I-MIBG là các thăm khám bổ sung để xác định vị trí khối u tủy thượng thận. Có thể đặt catheter chọn lọc để định lượng catecholamin máu tĩnh mạch thượng thận so sánh với catecholamin của máu tĩnh mạch các vị trí khác cũng là một xét nghiệm có ích.
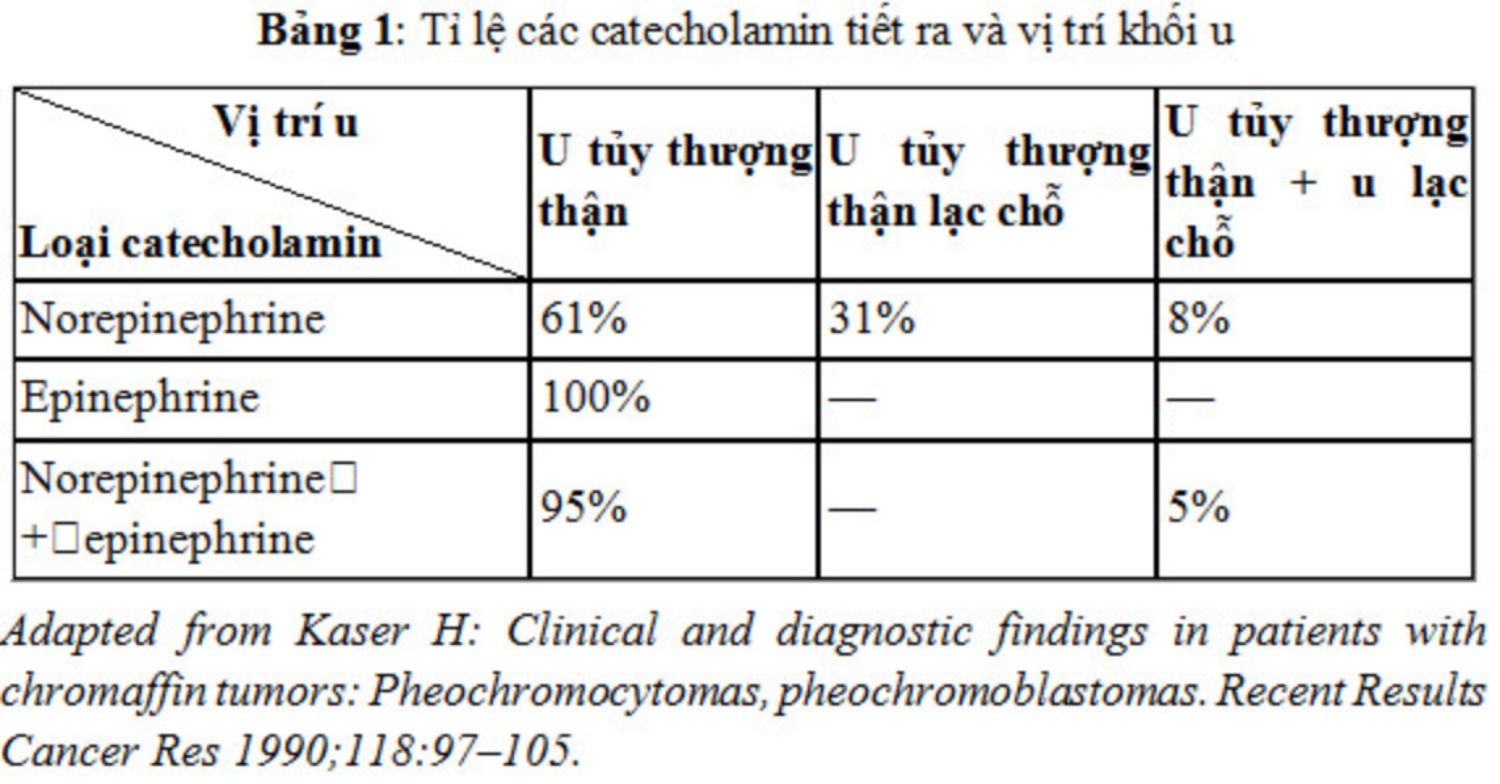
4. VÔ CẢM CHO PHẪU THUẬT
4.1. Giai đoạn chuẩn bị trước mổ
Không có các nghiên cứu có kiểm soát, tiến cứu ngẫu nhiên về ý nghĩa của việc ức chế hệ adrenergic ở những bệnh nhân u tủy thượng thận ở giai đoạn trước trong và sau mổ. Tuy nhiên, việc đưa vào sử dụng các thuốc ức chế anpha-adrenergic trong giai đoạn trước mổ, tỷ lệ tử vong sau cắt tủy thượng thận đã giảm từ 40%-60% năm 1951 xuống 0%-6% năm 1967. Kết quả này mang lại nhiều thuận lợi cho quá trình vô cảm và theo dõi vô cảm. Một số tác giả thấy sử dụng các thuốc tác dụng nhanh có ích lợi hơn sử dụng các thuốc ức chế anpha. Vì hầu hết các khối u tủy thượng thận tiết ra nhiều norepinephrin hơn epinephrin, điều trị nội khoa thuốc ức chế anpha làm hạ huyết áp, tăng thể tích nội mạch, ngăn ngừa các cơn tăng huyết áp kịch phát, làm tăng sự nhạy cảm của các receptor adrenergic và giảm rối loạn chức năng cơ tim. Mặc dù có thể u tủy thượng thận có thể kèm theo giảm đáng kể thể tích nội mạch, đa số các bệnh nhân có thể tích nội mạch bình thường hoặc giảm nhẹ. Các thuốc ức chế anpha có tác dụng bảo vệ hiệu quả co bóp cơ tim và việc tưới máu mô từ các tác dụng bất lợi của catecholamin. Phenoxybenzamin là thuốc ức chế anpha được sử dụng thường xuyên nhất giai đoạn trước mổ. Nó là thuốc ức chế không cạnh tranh chủ vận anpha 1 và có một số thuộc tính ức chế anpha 2. Vì là một chất ức chế không cạnh tranh nên nó rất khó để ức chế hết các catecholamin dư thừa. Phenoxybenzamin có thời gian tác dụng dài nên chỉ cần uống hai lần một ngày. Liều khởi đầu thường là 10 -20 mg, 2 lần mỗi ngày, hầu hết các bệnh nhân cần tới 60-250 mg /ngày. Mục tiêu điều trị là đưa huyết áp về bình thường, làm hết cá triệu chứng, hết sự biến đổi sóng ST và sóng T trên điện tim đồ và loại trừ rối loạn nhịp tim. Điều trị quá liều có thể gây hạ huyết áp tư thế đứng. Khoảng thời gian điều trị ức chế anpha bao lâu là tối ưu vẫn còn là dấu hỏi, nhìn chung dao động từ 2 đến 3 tuần hoặc lâu hơn. Bởi vì nó có tác dụng kéo dài trên receptor anpha nên khuyến cáo ngừng thuốc 24 đến 48 giờ trước phẫu thuật để tránh việc mất đáp ứng của mạch máu ngay sau khi lấy bỏ khối u. Một số bác sĩ gây mê chỉ sử dụng một nửa hoặc 2/3 liều buổi sáng trước cuộc mổ để có tác dụng tương tự. Trong khi phẫu thuật viên yêu cầu ngừng thuốc 48 giờ trước phẫu thuật để họ sử dụng việc tăng huyết áp trong mổ như là tín hiệu để xác định các khối u di căn. Tuy nhiên, cho dù có dùng đầy đủ các thuốc ức chế anpha trước mổ thì tăng huyết áp vẫn xảy ra khi kích thích bằng tay vào khối u. Nhưng do ức chế thụ cảm thể anpha 1 và anpha 2, phenoxybenzamin làm tăng tiết catecholamin thông qua việc ức chế anpha 2 gây nhịp tim nhanh.
Prazocin là thuốc ức chế cạnh tranh chọn lọc anpha 1 có thể được sử dụng thay thế phenoxybenzamin. Nó có thời gian tác dụng ngắn hơn, ít gây tăng nhịp tim hơn và dễ chuẩn độ hơn phenoxybenzamin. Liều khởi đầu là 1 mg, dùng 3 lần mỗi ngày, có thể tăng liều tới 8-12 mg/ngày để đạt được tác dụng mong muốn. Một số ý kiến cho rằng nó không ngăn chặn đầy đủ các cơn tăng huyết áp ở giai đoạn trước phẫu thuật mặc dù có nhiều ý kiến ủng hộ việc sử dụng prazocin. Các thuốc ức chế anpha 1 khác bao gồm doxazosin và terazosin. Doxazosin sử dụng liều từ 2 -6 mg/ngày có hiệu quả kiểm soát tăng huyết áp như phenoxybenzamin và gây ít tác dụng không mong muốn hơn ở giai đoạn trước mổ (nhịp tim nhanh) và sau mổ (giảm huyết áp) cắt bỏ khối u.
Sử dụng các thuốc ức chế beta-adrenergic thay thế nếu nhịp tim nhanh (>120 nhịp/phút) hoặc xuất hiện các rối loạn nhịp tim do tác dụng ức chế anpha 2 từ phenoxybenzamin. Các thuốc ức chế chọn lọc beta-adrenergic không bao giờ được sử dụng trước các thuốc ức chế anpha vì ức chế tác dụng giãn mạch của receptor beta 2 gây ra mất đối kháng với chủ vận anpha dẫn tới co mạch và tăng huyết áp. Propranolol là thuốc ức chế không chọn lọc beta 1, beta 2 có thời gian bán thải trên 4 giờ thường được sử dụng nhất. Hầu hết các bệnh nhân cần tới 80-120 mg/ngày. Một số bệnh nhân có u tủy thượng thận tiết ra epinephrin liều có thể dùng tới 480 mg/ngày. Các thuốc ức chế beta cần được sử dụng một cách cẩn trọng vì dù liều thấp nhưng có một số đáng kể bệnh nhân xuất hiện suy tim xung huyết hoặc bệnh lý cơ tim khi đã có sẵn các bệnh lý này nhưng ở trạng thái tiềm tàng. Atenolol, metoprolol và labetalol đã được sử dụng có hiệu quả, mặc dù kinh nghiệm về các thuốc này vẫn còn hạn chế và có một số thông báo biến chứng về sau. Labetalol gây ra mức độ ức chế anpha và beta (tác dụng ức chế beta nhiều hơn anpha) có thể không thích hợp cho bệnh nhân u tủy thượng thận. Rất ít khi lựa chọn sử dụng các thuốc ức chế beta trước khi sử dụng thuốc ức chế anpha. Với bệnh nhân u tủy thượng thận tiết ra epinephrin đơn thuần và có bệnh lý động mạch vành có thể có lợi ích lớn hơn khi dùng thuốc ức chế chọn lọc receptor beta 1 như esmolol. Esmelol có thời gian khởi phát tác dụng nhanh và thời gian bán thải ngắn, có thể dử dụng tiêm tĩnh mạch ngay trước khi phẫu thuật.
α-Methylparatyrosine (metyrosine) ức chế việc kiểm soát tốc độ quá trình tổng hợp catecholamin, làm giảm 50% đến 80% lượng catecholamin được tạo ra. Liều sử dụng thay đổi từ 250 mg cho tới 3 hoặc 4 g/ngày. Nó đặc biệt hiệu quả ở khối u ác tính mà không có chỉ định mổ. Tác dụng không mong muốn bao gồm phản xạ ngoại tháp và tinh thể niệu làm hạn chế việc sử dụng thuốc này. Khi phối hợp với phenoxybenzamin trong giai đoạn trước mổ, metyrosine có tác dụng tạo sự thuận lợi cho kiểm soát huyết động trong mổ.
Có thể sử dụng các thuốc ức chế kênh calci và thuốc ức chế men chuyển để kiểm soát tăng huyết áp. Calci là chất kích hoạt khối u tiết catecholamin và khi lượng lớn calci vào trong cơ tim góp phần gây ra bệnh lý cơ tim qua trung gian catecholamin. Phối hợp một thuốc ức chế beta 1 và một thuốc ức chế kênh calci (verapamil 120 mg – 240 mg mỗi ngày hoặc nifedipine 30 mg – 90 mg mỗi ngày) là một sự kết hợp có hiệu quả cho những trường hợp kháng thuốc.
4.2. Giai đoạn trong mổ
Các phẫu thuật có chuẩn bị được khuyến cáo bất cứ khi nào có thể. Chuẩn bị tối ưu trước mổ với thuốc ức chế anpha-adrenergic phối hợp hoặc không với thuốc ức chế beta-adrenergic và α-methylparatyrosin và cần điều trị hồi phục việc thiếu thể tích tuần hoàn. Mục tiêu của kiểm soát trong mổ bao gồm tránh sử dụng các thuốc hoặc các thao tác thô bạo có thể kích động tăng tiết catecholamin hoặc làm gia tăng tiềm lực hoạt động của catecholamin và duy trì sự ổn định về tim mạch với các thuốc tác dụng ngắn. Các thời điểm nguy hiểm nhất có thể gây tăng huyết áp thứ phát kèm theo rối loạn nhịp là lúc khởi mê, đặt ống nội khí quản, rạch da, mở bụng và đặc biệt trong khi lôi kéo khối u. Thời điểm buộc thắt tĩnh mạch của khối u cũng rất nguy hiểm vì gây hạ huyết áp thứ phát. Theo dõi trong quá trình mổ gồm thiết bị theo dõi chuẩn cộng với theo dõi huyết áp động mạch xâm lấn, áp lực tĩnh mạch trung tâm, áp lực động mạch phổi qua catheter động mạch phổi và đặt sonde niệu đạo theo dõi nước tiểu. Nếu có thể theo dõi siêu âm tim qua thực quản để đánh giá chức năng cơ tim. Catheter động mạch cho phép theo dõi huyết áp động mạch dựa trên nhịp cơ bản, hơn nữa có thể lấy máu động mạch để làm các xét nghiệm cần thiết (như xét nghiệm hematocrit, hemoglobin, khí máu động mạch, đường máu). Một catheter tĩnh mạch trung tâm thường là đủ cho các bệnh nhân không có triệu chứng ở hệ tim mạch hoặc các dấu hiệu khác liên quan đến tim mạch. Catheter động mạch phổi có thể cần thiết để kiểm soát khi truyền một lượng dịch lớn, thiếu nhiều thể tích tuần hoàn và ở những bệnh nhân rối loạn chức năng cơ tim tiềm ẩn với các khối u hoạt động. Một lượng dịch lớn cần bù vào sau khi khối u được cắt bỏ cho thấy giảm mối quan hệ giữa thể tích và huyết áp do giảm đột ngột lượng catecholamin. Cần đảm bảo một lượng dịch trong cân bằng dương lớn để giữ thể tích nội mạch ở trong giới hạn bình thường.
Có thể sử dụng siêu âm trong mổ để xác định vị trí và chức năng các khối u nhỏ và để thực hiện việc tách tuyến thượng thận hoặc cắt bán phần tuyến thượng thận. Quá trình tách tuyến thượng thận thực sự có giá trị khi cắt bỏ u ở tuyến thượng thận hai bên. Phẫu thuật nội soi có thể được thực hiện khi kích thước khối u nhỏ hơn 4 cm -5 cm. Thường gặp tăng huyết áp khi bơm hơi ổ bụng cũng như khi kích thích trực tiếp vào khối u.
Cả hai kỹ thuật vô cảm vùng và gây mê toàn thể đều đã được áp dụng thành công cho phẫu thuật cắt u tuyến thượng thận. Các thuốc có thể gây đáp ứng tăng huyết áp thông qua:
- Kích thích trực tiếp các tế bào khối u.
- Kích thích hệ thần kinh giao cảm.
- Tăng giải phóng các catecholamin dự trữ ở các tận cùng thần kinh.
- Can thiệp vào sự thu nhận catecholamin của tế bào thần kinh.
- Gây mẫn cảm các receptor catecholamin hoặc làm tăng hiệu quả tác dụng của catecholamin lên các tiểu động mạch.
Tất cả các thuốc gây mê đều đã được sử dụng với mức độ thành công khác nhau, về mặt lý thuyết một số thuốc cần tránh sử dụng để ngăn chặn đáp ứng bất lợi về mặt huyết động có thể xảy ra. Morphin và atracurium có thể gây tăng tiết histamin, có thể là yếu tố thúc đẩy tăng tiết catecholamin từ khối u. Các thuốc hủy phó giao cảm như atropin, pancuronium (Pavulon) và succinylcholin hoặc các thuốc kích thích thần kinh giao cảm đều có thể gây kích thích hệ thần kinh giao cảm. Mặc dù nồng độ cao halothan có hiệu quả cao trong việc làm suy giảm các đáp ứng biến đổi huyết động (như tăng huyết áp, tăng nhịp tim) với các kích thích vô cảm và phẫu thuật, nhưng nó lại làm tăng độ nhạy cảm của cơ tim với catecholamin nên cần tránh sử dụng. Droperidol, chlorpromazine, metoclopramide và ephedrin gây đáp ứng tăng huyết áp đáng kể. Các thuốc gây mê an toàn gồm thiopental, etomidate, các benzodiazepine, fentanyl, sufentanil, alfentanil, enfluran, isofluran, nitrous oxide, vecuronium và rocuronium. Mặc dù vậy, nhưng việc lựa chọn các thuốc gây mê không quan trọng bằng sự hiểu biết về thuốc nào sẽ được sử dụng. Các yếu tố kích thích tăng tiết catecholamin như là sự sợ hãi, căng thẳng, đau, run rẩy, thiếu oxy và tăng thán khí cần được giảm tới mức thấp nhất hoặc tránh ở giai đoạn trước, trong và sau mổ.
Gần như tất cả các bệnh nhân đều có biểu hiện tăng huyết áp động mạch tâm thu trên 200 mmHg giai đoạn trong mổ cho dù đã dùng thuốc ức chế anpha từ trước mổ. Cần chuẩn bị một số thuốc hạ huyết áp và sẵn sàng sử dụng ngay khi cần thiết. Muối nitroprusside, một thuốc giãn mạch trực tiếp là thuốc được lựa chọn vì hiệu lực và khởi phát tác dụng ngay sau khi tiêm, thời gian tác dụng ngắn. Phentolamin, thuốc ức chế cạnh tranh anpha-adrenergic và gây giãn mạch trực tiếp rất hiệu quả mặc dù giảm nhanh tác dụng và gây nhịp chậm tim. Nitroglycerin cũng có hiệu quả nhưng nó đòi hỏi liều cao để kiểm soát những cơn tăng huyết áp và có thể gây nhịp nhanh tim. Labetalol có tác dụng ức chế beta nhiều hơn ức chế anpha được sử dụng nhiều hơn ở những bệnh nhân có khối u tăng tiết ưu thế epinephrin. Magnesium sulfat ức chế tiết catecholamin từ u tủy thượng thận và tận cùng thần kinh ngoại vi, làm giảm sự nhạy cảm của các receptor anpha với catecholamin và có tác dụng giãn mạch trực tiếp cũng như chống rối loạn nhịp tim. Tuy nhiên, cũng như các thuốc điều trị tăng huyết áp khác, nó không đạt được sự kiểm soát tăng huyết áp tối ưu khi kích thích khối u tủy thượng thận bằng tay. Sự phối hợp các thuốc điều trị tăng huyết áp như là nitroprusside, esmolol, diltiazem và phentolamine được sử dụng để kiểm soát tăng huyết áp khó điều trị. Tăng độ sâu gây mê cũng là một sự lựa chọn mặc dù điều này có thể làm nặng thêm hạ huyết áp khi kẹp cắt tĩnh mạch khối u.
Rối loạn nhịp tim thường là xuất phát từ thất và được điều trị bằng lidocain hoặc các thuốc ức chế beta. Lidocain có tác dụng ngắn và ít ảnh hưởng tới sự co bóp cơ tim. Mặc dù propranolol được sử dụng rộng rãi nhưng esmolol (ức chế chọn lọc beta 1) mới là thuốc có nhiều ưu điểm hơn. Esmolol khởi phát tác dụng nhanh và thời gian tác dụng ngắn (thời gian bán thải là 9 phút), cho phép kiểm soát thích hợp nhịp tim và có tác dụng bảo vệ chống lại bệnh cơ tim và thiếu máu cơ tim do catecholamin cũng như chống lại sự hạ đường máu sau mổ. Amiodaron là thuốc chống loạn nhịp có tác dụng kéo dài điện thế hoạt động của cơ nhĩ và thất đã được sử dụng như thuốc thay thế ức chế beta (metoprolol) để điều trị nhịp nhanh trên thất do tăng cao catecholamin.
Thường có tụt huyết áp đáng kể sau khi kẹp thắt tĩnh mạch khối u và thứ phát do sự kết hợp của các yếu tố bao gồm như giảm đột ngột nồng độ catecholamin huyết tương (nửa đời sống thải trừ của norepinephrine và epinephrine khoảng từ 1 – 2 phút), giãn mạch do tồn dư các thuốc ức chế anpha cùng với phenoxybenzamin, mất máu và dịch trong mổ và tăng độ sâu của gây mê. Huyết áp tâm thu tụt dưới 70 mmHg không thường xảy ra. Để dự phòng tụt huyết áp đột ngột, cần nâng áp lực giường mao mạch phổi lên 16 đến 18 mmHg trước khi kẹp cắt tĩnh mạch u thượng thận. Thường sử dụng dung dịch ringer lactat hoặc nước muối sinh lý trước khi lấy bỏ khối u và bổ sung dung dịch dextrose sau khi cắt u. Cần giảm độ sâu gây mê để góp phần kiểm soát huyết áp thấp. Sau khi cắt u thượng thận gây ra hiện tượng giảm đột ngột nồng độ catecholamin huyết tương, kéo theo tăng mức insulin và giảm đường máu. Thường ít gây mất máu khi cắt u tuyến thượng thận trong ổ bụng. Các thuốc co mạch (như phenylephrine, norepinephrine) và tăng sức bóp cơ tim (dopamine) cần sẵn sàng sử dụng nếu huyết áp thấp chậm đáp ứng với liệu pháp truyền dịch. Cần thiết bổ sung một lượng dịch thích hợp và đó là yếu tố chính làm giảm tỷ lệ tử vong trong mổ u tuyến thượng thận. Các thuốc co mạch và tăng cường sức bóp cơ tim cần được xem như một phương thức điều trị thứ cấp. Sự tồn dư các thuốc ức chế anpha-adrenergic và giảm sự điều hòa các receptor khiến một số bệnh nhân ít đáp ứng với thuốc co mạch. Liệu pháp glucocorticoid cần được áp dụng nếu thực hiện cắt u tuyến thượng thận hai bên hoặc có khả năng suy tuyến thượng thận.
4.3. Giai đoạn sau mổ
Phần lớn các bệnh nhân có huyết áp trở lại bình thường sau khi cắt bỏ hoàn toàn khối u. Mức catecholamin huyết tương chưa trở về bình thường cho tới tận ngày thứ 7 hoặc 10 sau mổ do có sự giải phóng dần dần catecholamin từ tận cùng các sợi thần kinh ngoại vi. Có khoảng 50% bệnh nhân tăng huyết áp một vài ngày sau mổ, có 25% – 30% bệnh nhân tăng huyết áp không hạn định. Tăng huyết áp này thường thấp hơn so với trước phẫu thuật và không có cơn tăng huyết áp kịch phát và không có các triệu chứng kinh điển của tăng catecholamin trong máu. Chẩn đoán phân biệt các bệnh nhân có tăng huyết áp dai dẳng với trường hợp chẩn đoán nhầm u tủy thượng thận, thiếu máu thận sau biến chứng của phẫu thuật và những bệnh nhân tăng huyết áp tiềm tàng.
Tụt huyết áp là nguyên nhân thường gặp nhất gây tử vong ngay trong giai đoạn sau phẫu thuật. Cần bổ sung lượng lớn dịch truyền vì các mạch máu ngoại vi không đáp ứng với giảm mức catecholamin. Hơn nữa, có sự mất dịch vào khoang thứ ba, tác dụng của phenoxybenzamine và α-methylparatyrosine tồn dư có thể kéo dài thời gian bán thải tới 36 giờ. Cần bổ sung steroid cho các bệnh nhân cắt u tuyến thượng thận hai bên hoặc nghi ngờ có suy tuyến thượng thận.
Có thể hạ đường máu vì tăng tiết quá mức insulin và phân giải mỡ, glycogen không thích hợp. Các thuốc ức chế không chọn lọc beta như propranolol có thể làm trầm trọng thêm việc hạ đường máu do giảm trương lực giao cảm và che giấu các triệu chứng của hạ đường máu. Truyền dung dịch chứa dextrose được coi là một phần trong truyền dịch liệu pháp và mức glucose máu cũng cần được theo dõi 24 giờ.
Các bệnh nhân thường được lưu lại ICU ít nhất 24 giờ. Cần có chế độ kiểm soát đau thích hợp mặc dù có sự tăng nhạy cảm với các thuốc giảm đau morphin và ngủ gà. Nhu cầu kiểm soát thông khí dựa trên mức độ của phẫu thuật, vị trí phẫu thuật và tình trạng của bệnh nhân.
5. KẾT LUẬN
Tỷ lệ mắc bệnh có liên quan tới cắt bỏ u tuyến thượng thận khoảng 24% và tỷ lệ tử vong khoảng 2,4%. Sự hiểu biết sâu sắc về sinh lý bệnh khối u tủy thượng thận là điều quan trọng nhất để dự kiến kế hoạch vô cảm. Những tiến bộ mới đây về phương pháp chẩn đoán và định vị khối u cũng như sự phát triển các thuốc mới điều trị hạ huyết áp trong tương lai sẽ góp phần chăm sóc và điều trị tốt hơn cho các bệnh nhân u tủy thượng thận. Chuẩn bị bệnh nhân kỹ lưỡng trước mổ; có sự phối hợp tốt giữa bác sĩ nội khoa, bác sĩ nội tiết, phẫu thuật viên và bác sĩ gây mê; chuẩn bị đầy đủ và tỉ mỉ trong khi mổ; kiểm soát tốt tình trạng trước, trong và sau mổ là những điều cần thiết để thực hiện quá trình vô cảm phẫu thuật cho bệnh nhân u tủy thượng thận.
Vô cảm hồi sức trong phẫu thuật tiết niệu
1. VÔ CẢM CHO CÁC PHẪU THUẬT NIỆU KHOA ĐẶC BIỆT
1.1. Nội soi bàng quang và nội soi niệu quản: được thực hiện để chẩn đoán và điều trị các tổn thương phần thấp (niệu đạo, tiền liệt tuyến và bàng quang) và phần cao (niệu quản, thận) của đường tiết niệu.
1.1.1 Sử dụng dung dịch tưới rửa: ấm giúp nhìn rõ và loại bỏ máu, mô và các mảnh sỏi
- Dung dịch rửa điện giải: như nước muối sinh lý và Ringerlactat là đẳng trương và không gây tan huyết khi hấp thụ vào lòng mạch. Bởi vì có chứa các ion nên dung dịch này không an toàn khi sử dụng cho các thủ thuật có liên quan đến dao điện
- Nước cất: giúp nhìn tối ưu và không dẫn điện. Tuy nhiên, khi hấp thu lòng mạch có thể gây ra tan huyết và giảm natri máu/ giảm độ thẩm thấu.
- Dung dịch không điện giải: glycine, sorbitol, manitol giúp nhìn tốt và không dẫn điện. Dung dịch này gần đẳng trương giảm thiểu tan huyết , mặc dù hấp thu một số lượng lớn nước có thể gây ra giảm natri máu (không giảm đáng kể độ thẩm thấu).
1.1.2. Vô cảm:
- Tùy thuộc vào bệnh nhân và phẫu thuật, vô cảm cho nội soi bàng quang/nội soi niệu quản có thể chỉ sử dụng thuốc tê dạng gel tới gây tê tại chỗ hoặc gây tê vùng/gây mê. Việc đặt nội soi ống cứng bàng quang (đặc biệt ở đàn ông) và căng giãn bàng quang, niệu quản có thể khá kích thích. Tuy nhiên đau sau mổ là tối thiểu.
- Nếu sử dụng gây tê vùng, cần đạt mức T6 khi đặt các dụng cụ ở đường niệu trên, trong lúc mức T10 là đủ cho phẫu thuật đường niệu thấp.
- Gây mê có thể hiệu quả bằng các loại thuốc mê tĩnh mạch tác dụng ngắn hoặc thuốc mê bốc hơi. Giãn cơ thoáng qua có thể cần nếu thao tác trên các tổn thương bàng quang gần dây thần kinh bịt gây ra cử động chân không tự chủ.
- Tư thế mở bàng quang gắp sỏi là tư thế phổ biến.
1.2. Cắt bỏ tiền liệt tuyến qua niệu đạo (TURP):
Được thực hiện ở nam giới cao tuổi để điều trị tắc nghẽn đường niệu do bởi phì đại lành tính tuyến tiền liệt. Phẫu thuật này sử dụng bộ nội soi bàng quang cải biên (ống soi cắt đoạn) với quai kim loại kết nối với dao điện để cắt bỏ mô và cầm máu..
1.2.1. Trong phẫu thuật: các xoang tĩnh mạch lớn tiền liệt tuyến tổn thương dẫn đến hấp thu nước tưới rửa. Lượng dịch hấp thu phụ thuộc vào các yếu tố sau:
- Áp lực thủy tĩnh dung dịch tưới rửa, tỷ lệ với độ cao của bình tưới rửa đặt phía trên bệnh nhân.
- Kỹ thuật phẫu thuật: thời gian phẫu thuật, tốc độ dòng tưới rửa, kích cỡ bộ nội soi bàng quang.
- Số lượng và kích cỡ xoang tĩnh mạch bị tổn thương (bị ảnh hưởng bởi kích cỡ tiền liệt tuyến).
- Áp lực tĩnh mạch ngoại vi (áp lực thấp hơn gây tăng hấp thu)
1.2.2. Vô cảm:
- Nếu sử dụng gây mê, cần thiết phòng ngừa ho hoặc cử động của bệnh nhân, điều này có thể gây ra tăng chảy máu hoặc thủng bàng quang/thủng bao tiền liệt tuyến. Thông khí áp lực dương có thể giảm hấp thu dịch rửa bằng việc tăng áp lực tĩnh mạch.
- Lợi ích gây tê vùng có thể bao gồm mất trương lực bàng quang (giúp trường mổ nhìn rõ hơn) và loại bỏ co thắt bàng quang (cầm máu sau mổ nhanh hơn). Thêm vào đó, bệnh nhân thức tỉnh có thể thông báo các triệu chứng cho phép phát hiện sớm hơn hội chứng TURP hoặc thủng bàng quang.
- Gây tê tủy sống có thể sử dụng dung dịch thuốc tê ưu tỷ trọng có hay không có opioid, đủ giảm đau với ảnh hưởng huyết động tối thiểu. Một số tác giả khuyến cáo mức T10 bởi vì có thể đau do căng giãn bàng quang. Áp lực tĩnh mạch thấp hơn kết hợp với phong bế trục não tủy có thể giảm chảy máu nhưng tăng hấp thu dịch tưới rửa.
- Các phương pháp theo dõi hấp thu dịch trong mổ bao gồm cân bằng thể tích dịch, cân nặng trọng lượng và đo ethanol hơi thở khi đã biết số lượng ethanol được bổ sung vào dịch tưới rửa.
1.2.3. Các biến chứng:
– Hội chứng TURP: liên quan tới tập hợp các triệu chứng thần kinh và tim mạch và các dấu hiệu gây ra bởi hấp thu dịch rửa quá mức. Nó có thể xuất hiện sớm (hấp thu mạch máu trực tiếp) hoặc sau một vài giờ (hấp thu từ các khoang sau phúc mạc và quanh túi tinh). Hội chứng này cũng có thể gặp trong phẫu thuật nội soi tử cung.
- Các thay đổi ở hệ thần kinh trung ương: bao gồm buồn nôn, kích thích, nhầm lẫn, biến đổi thị lực, co giật, hôn mê. Các ảnh hưởng này dường như do nhiều yếu tố và được quy cho giảm natri máu/giảm độ thẩm thấu dẫn đến phù não, tăng glycin máu/tăng ammonia máu (glycin được chuyển hóa ở gan thành ammonia) kết hợp với dung dịch glycine và các thuốc an thần dùng kèm.
- Các dấu hiệu tim mạch: bao gồm tăng hoặc giảm huyết áp, nhịp tim chậm, loạn nhịp tim, phù phổi, ngừng tim, dường như thứ phát do chuyển dịch mạnh dịch thể và kết hợp với rối loạn điện giải. Ban đầu xảy ra tăng khối lượng máu lưu hành với hấp thu dịch, theo sau bởi tái phân bố nhanh của dịch rửa vào khoảng kẽ.
- Thông báo ngay cho phẫu thuật viên và hoàn tất phẫu thuật càng nhanh càng tốt và điều trị biến đổi huyết động. Người ta vẫn chưa thống nhất trong y văn về liệu pháp điều trị thích hợp nhất. Người ta tán thành hạn chế dịch truyền và sử dụng lợi niệu furosemide để điều trị quá tải dịch, sử dụng dung dịch muối ưu trương cho các triệu chứng nguy kịch hoặc giảm natri máu (nồng độ natri huyết tương <120mmol/L). Các tác giả khác đề xuất rằng chiến lược lợi niệu có thể làm nặng thêm tình trạng mất nước lòng mạch, giảm natri máu và khuyến cáo sử dụng sớm muối ưu trương (với hiệu chỉnh chậm giảm natri máu để giảm thiểu nguy cơ của hủy myelin cầu não), sử dụng lợi niêu khi xuất hiện phù phổi cấp. Trong bất cứ trường hợp nào, liệu pháp điều trị nên được hướng dẫn bởi đo lường đều đặn nồng độ natri huyết tương và độ thẩm thấu.
– Thủng bàng quang:
- Thủng ngoài phúc mạc thường gặp hơn và biểu lộ như là căng phồng trên khớp mu, co thắt bụng, hoặc đau ở trên khớp mu, bẹn hoặc quanh rốn.
- Thủng trong phúc mạc biểu lộ như đau bụng trên hoặc đau ở vùng quy chiếu từ cơ hoành tới vai, điều này có thể dẫn đến cao huyết áp, nhịp tim nhanh, chướng bụng, theo sau bởi hạ huyết áp và suy tuần hoàn.
– Nhiễm trùng huyết: dường như do bởi hấp thu vi khuẩn qua các xoang tĩnh mạch tiền liệt tuyến, thường kết hợp với đặt sonde tiểu hoặc viêm tiền liệt tuyến điều trị chưa đầy đủ.
– Mất máu và bệnh lý đông máu: đánh giá mất máu là rất khó trong TURP bởi vì hòa loãng lượng lớn do dịch rửa
- Chảy máu tiếp tục sau mổ có thể do bởi giảm tiều cầu pha loãng, đông máu rải rác nội mạch, hoặc phóng thích các men tiêu fibrin từ tiền liệt tuyến.
- Đáp ứng huyết động với mất máu có thể bị che phủ bởi tăng khối lượng máu lưu hành từ hấp thu dịch rửa.
– Các biện pháp điều trị khác TURP: bao gồm sử dụng thuốc (phong bế alpha, liệu pháp điều trị hormon) và các kỹ thuật xâm lấn tối thiểu mới hơn bao gồm cắt bỏ bằng lase, liệu pháp điều trị nhiệt vi sóng và đặt stent tiền liệt tuyến. Mặc dù các phẫu thuật này chưa được so sánh với TURP trong các nghiên cứu tiến cứu lớn nhưng người ta tán thành sử dụng chúng cho các bệnh nhân mắc các bệnh kết hợp có nguy cơ cao các biến chứng phẫu thuật và vô cảm.
1.3. Mổ mở tiền liệt tuyến: được thực hiện để cắt bỏ khối tiền liệt tuyến lớn, thường gặp hơn là do u.
1.3.1. Vô cảm:
– Phẫu thuật này có thể được thực hiện an toàn dưới gây mê toàn thể, gây mê toàn thể kết hợp gây tê ngoài màng cứng, gây tê ngoài màng cứng hoặc gây tê tủy sống. Một số thử nghiệm ngẫu nhiên tiến cứu số lượng nhỏ so sánh gây mê toàn thể với gây tê ngoài màng cứng đã nhận thấy lợi ích vừa phải của gây tê ngoài màng cứng trong việc giảm mất máu, giảm đau sau mổ, hồi phục nhanh chức năng ruột, trong lúc các nghiên cứu khác cho thấy sự khác biệt đôi chút trong kết quả. Tuy nhiên bất kỳ lợi ích nào cũng phải so sánh với nhận xét rằng các phẫu thuật viên lành nghề thực hiện thường quy cắt bỏ tiền liệt tuyến dưới gây mê với mất máu tối thiểu, kiểm soát tốt đau trong mổ bằng opioid và các thuốc giảm đau chống viêm non-steroid sau mổ, ngày nằm viện ngắn với thời gian xuất viện sớm ngày thứ nhất sau mổ.
– Nhuộm chẩn đoán có thể được sử dụng trong phẫu thuật để chứng minh sự toàn vẹn của đường niệu được tái cấu trúc.
- Tiêm xanh methylen 1% (1mL) bolus có thể gây hạ huyết áp. Nó cũng có thể gây giảm sai sót thoáng qua SaO2 thấp tới 65% kéo dài 10 tới 70 giây.
- Tiêm indigocarmine 0,8& (5mL), chất chủ vận alpha. có thể gây tăng huyết áp.
– Đo lượng nước tiểu bị gián đoạn trong khi chuyển động của niệu đạo tiền liệt tuyến.
1.3..2. Biến chứng:
Nói chung liên quan tới mất máu, bao gồm hạ thân nhiệt, thiếu máu, bệnh lý đông máu. Người ta khuyên dùng nên đặt kim luồn nòng lớn.
1.4. Cắt thận:
Được thực hiện với u, ghép thận, nhiễm trùng thận mãn, chấn thương và bệnh nang thận hoặc sỏi thận nặng.
1.4.1. Bệnh nhân trải qua cắt thận với u tế bào thận: yêu cầu giai đoạn chuẩn bị trước mổ. Nếu khối u xâm lấn vào tĩnh mạch chủ dưới hoặc nhĩ phải, hai biến chứng sau có thể xảy ra:
- Khối u có thể gây bít tắc một phần hoặc hoàn toàn tĩnh mạch chủ dưới: dẫn đến ứ đọng máu tĩnh mạch trở về và giảm huyết áp. Cắt toàn bộ khối u có thể cần thiết kẹp tạm thời tĩnh mạch chủ dưới kèm theo gia tăng giảm máu tĩnh mạch trở về yêu cầu sử dụng thuốc vận mạch. Siêu âm ngả qua thực quản trong mổ có thể được sử dụng để theo dõi huyết khối u.
- Các mảnh của khối u có thể gây tắc mạch phổi: do đó đặt catheter động mạch phổi là đầy mạo hiểm nếu vị trí catheter đẩy khối u vào trong tĩnh mạch chủ dưới hoặc nhĩ phải. Có thể sử dụng tuần hoàn ngoài cơ thể để giảm thiểu nguy cơ của tắc mạch phổi trong mổ.
1.4.2. Vô cảm:
- Bệnh nhân nắm ngửa nếu tiếp cận đường bụng hoặc nghiêng nếu tiếp cận sau phúc mạc.
- Có thể cần đường rạch bụng ngực với khối u lớn hoặc ở cực trên
- Gây mê toàn thể phối hợp gây tê ngoài màng cứng thường được sử dụng để giảm đau tối đa sau mổ với đường rạch bụng trên hoặc đường rạch bụng ngực.
- Cần đặt kim luồn nòng lớn vào tĩnh mạch có hay không có đường động mạch khi mất máu nhiều bởi vì kích cỡ và sự phân bố mạch máu của khối u.
1.5. Cắt bỏ tiệt căn bàng quang:
Có hay không ống dẫn hồi tràng hoặc kết tràng được thực hiện cho khối u bàng quang xâm lấn. Các bệnh nhân khác với khối u ác tính xương chậu, rối loạn chức năng bàng quang nguồn gốc thần kinh, tắc nghẽn đường niệu thấp mãn tính hoặc rối loạn chức năng bàng quang sau chiếu xạ có thể yêu cầu phẫu thuật chuyển hướng đường niệu hồi tràng hoặc kết tràng
1.5.1. Vô cảm:
- Đặt kim luồn tĩnh mạch nòng lớn là bắt buộc vì mất máu đáng kể có thể xảy ra.
- Đặt catheter động mạch hoặc tĩnh mạch trung ương khi có chuyển dịch lớn dịch thể trong khi niệu quản không được kết nối
- Nên phối hợp gây mê toàn thể với gây tê ngoài màng cứng.
1.6. Cố định tinh hoàn, cắt bỏ tinh hoàn, phẫu thuật tạo hình niệu sinh dục:
Được thực hiện để điều trị dị dạng bẩm sinh, u và liệt dương. Bệnh nhân bị xoắn tinh hoàn có thể yêu cầu cắt bỏ cấp cứu và cố định tinh hoàn ngăn ngừa thiếu máu. Gây tê vùng cần đạt mức giảm đau T9.
1.7. Phẫu thuật nội soi ổ bụng
Đang được sử dụng ngày càng nhiều cho các phẫu thuật mổ mở truyền thống bao gồm cắt bỏ tiền liệt tuyến, cắt thận, cắt bàng quang, tạo hình bể thận và lấy sỏi. Các đường vào nội soi ổ bụng truyền thống được sử dụng trong một số phẫu thuật yêu cầu đường rạch nhỏ. Hệ thống robot có thể được sử dụng để kiểm soát camera. Đặc biệt cắt u tiền liệt tuyến nội soi ổ bụng được thúc đẩy vì xâm lấn tối thiểu và kết quả lâm sàng tương đương với mổ mở mặc dù vẫn chưa có so sánh với mổ mở trong các thử nghiệm đối chứng ngẫu nhiên thời gian dài. Những lưu ý về gây mê tương tự như trong phẫu thuật nội soi ổ bụng nói chung hoặc sản khoa. Bơm khí cacbonic sau phúc mạc có thể kết hợp với tăng hấp thu toàn thân so với bơm khí cacbonic trong phúc mạc, mặc dù các báo cáo vẫn còn mâu thuẫn.
1.8. Ghép thận
Được thực hiện cho các bệnh nhân suy thận giai đoạn cuối. Người nhận thường mắc bệnh cao huyết áp và hoặc đái tháo đường. Người nhận có nguy cơ gia tăng bệnh mạch vành, suy tim xung huyết. Phải chú ý rối loạn điện giải, cân bằng axit bazơ, thiếu máu, rối loạn chức năng tiểu cầu thường gặp ở bệnh nhân ure huyết cao. Nếu có thể nên chạy thận trước mổ để giảm kali máu và hiệu chỉnh rối loạn cân bằng axit-bazơ.
1.8.1. Vô cảm
- Đặt đường truyền tĩnh mạch có lẽ khó khăn và tránh đặt ở các chỗ rò hoặc shunt, lợi ích của theo dõi xâm lấn bổ sung (đường động mạch hoặc tĩnh mạch trung ương) nên cân nhắc nguy cơ nhiễm khuẩn huyết liên quan catheter ở bệnh nhân suy giảm miễn dịch.
- Các thuốc chuyển hóa chủ yếu ở thận nên tránh hoặc giảm liều.
- Bệnh nhân đái tháo đường, ure huyết cao, sử dụng opioid trước mổ có thời gian rỗng dạ dày chậm.
- Tăng kali máu chống chỉ định dùng succinylcholine.
- Gây tê vùng có lẽ chống chỉ định bởi bệnh lý đông máu.
- Huyết thanh mặn đẳng trương có lẽ được ưa thích hơn Ringerlactat khi có kali máu tăng.
- Chức năng thận ghép tùy thuộc vào thể tích dịch lòng mạch đầy đủ trước và sau khâu nối mạch máu để duy trì tưới máu thận ghép. Các dung dịch giãn nở thể tích lòng mạch hữu ích gồm dịch tinh thể, albumin, mannitol.
- Huyết áp thấp trong mổ có thể gây tổn hại tưới máu thận và nên được điều trị mau lẹ bằng các biện pháp cơ học như ấn tĩnh mạch chủ dưới (IVC) hoặc điều trị giảm khối lượng máu lưu hành bằng truyền dịch. Sử dụng thuốc vận mạch nếu cần, inotropes (dopamine, dobutamine) được ưa thích hơn các thuốc tác động lên thụ thể alpha (phenylephrine, norepinephrine) có thể nâng huyết áp nhưng giảm dòng máu thận bởi co mạch. Trong trường hợp nhiễm toan máu nặng thì dùng natribicarbonat có thể cải thiện huyết động.
- Số lượng nước tiểu sớm cho biết chức năng thận, nhưng nó có thể bị ảnh hưởng bởi giảm khối lượng máu lưu hành, thải ghép cấp, hoặc sự lưu thông của mạch máu khâu nối. Cả mannitol và furosemid có thể được dùng để thúc đẩy lợi niệu sau khâu nối mạch máu.
2. TÁN SỎI NGOÀI CƠ THỂ (ESWL)
2.1. Nguyên lý: ESWL tập trung sóng âm vào viên sỏi đường niệu. Tại thiết diện giữa các vật liệu có mật độ khác nhau như giữa mô mềm và các viên sỏi, sự phản xạ của các sóng âm tạo ra mô hình phức tạp của siêu âm bên trong dẫn đến viên sỏi bị vỡ ra. Trong lúc các máy tán sỏi thế hệ đầu yêu cầu nhúng bệnh nhân vào bồn tắm thì các máy hiện nay cho phép bệnh nhân nằm trên bàn mổ và khu vực đi vào của shock qua da nhỏ hơn.
2.2. Vô cảm:
- Bệnh nhân nói chung nằm ngửa nhưng có thể nằm sấp: tuỳ thuộc vị trí chính xác của viên sỏi. Tư thế mở bàng quang gắp sỏi có lẽ cần thiết cho soi bàng quang hoặc đặt stent.
- Gây tê tại chỗ (monitored anesthesia care) thường đủ: với các máy tán sỏi đời mới vì chúng ít gây đau hơn các máy đời đầu. Giảm đau đầy đủ nói chung có thể bằng sử dụng opioid tĩnh mạch tác động ngắn như remifentanil, alfentanil với an thần bổ sung chuẩn độ theo đáp ứng của bệnh nhân. Nhiều chiến lược khác được sử dụng thành công bao gồm gây tê vùng và gây mê toàn thể.
- Truyền dịch đầy đủ: với lợi niệu bổ sung có thể hỗ trợ cho tống sỏi.
- Chống chỉ định tuyệt đối: có thai, nhiễm trùng chưa điều trị hoặc tạng chảy máu, và pacemaker ổ bụng. Chống chỉ định tương đối là pacemaker/đông máu rải rác nội mạch, phình động mạch thận hoặc động mạch chủ bụng, chân tay giả và béo bệnh lý.
2.3. Biến chứng:
- Cơn đau niệu quản sớm: ngay sau thủ thuật có thể biểu lộ buồn nôn, nôn, nhịp tim chậm.
- Đái máu: thường gặp và điều trị bằng truyền dịch và lợi niệu
- Loạn nhịp tim: như nhịp chậm, ngoại tâm thu nhĩ, ngoại tâm thu thất xảy ra trong phẫu thuật. Nếu ngoại tâm thu thất xảy ra thường xuyên hoặc có triệu chứng thì chúng có thể được giảm thiểu bởi đồng bộ hóa giữa sóng shock với chu chuyển tim.
- Tụ máu thận (dưới nang): có thể do bởi tổn thương mạch máu thận, đặc biệt ở bệnh nhân cao huyết áp
- Cao huyết áp: xảy ra chủ yếu ở bệnh nhân rối loạn phản xạ tự chủ
- Tổn thương ruột hoặc phổi nặng: hiếm gặp và xảy ra nếu sóng shock vô tình tác động trên phổi hoặc ruột, có thể xảy ra với cử động của bệnh nhân trong điều trị.
500 quy trình kỹ thuật gây mê hồi sức
Hướng dẫn chẩn đoán và điều trị một số bệnh thường gặp ở trẻ em - Bộ y tế 2015
Hướng dẫn quy trình kỹ thuật Phục hồi chức năng - Bộ y tế 2017
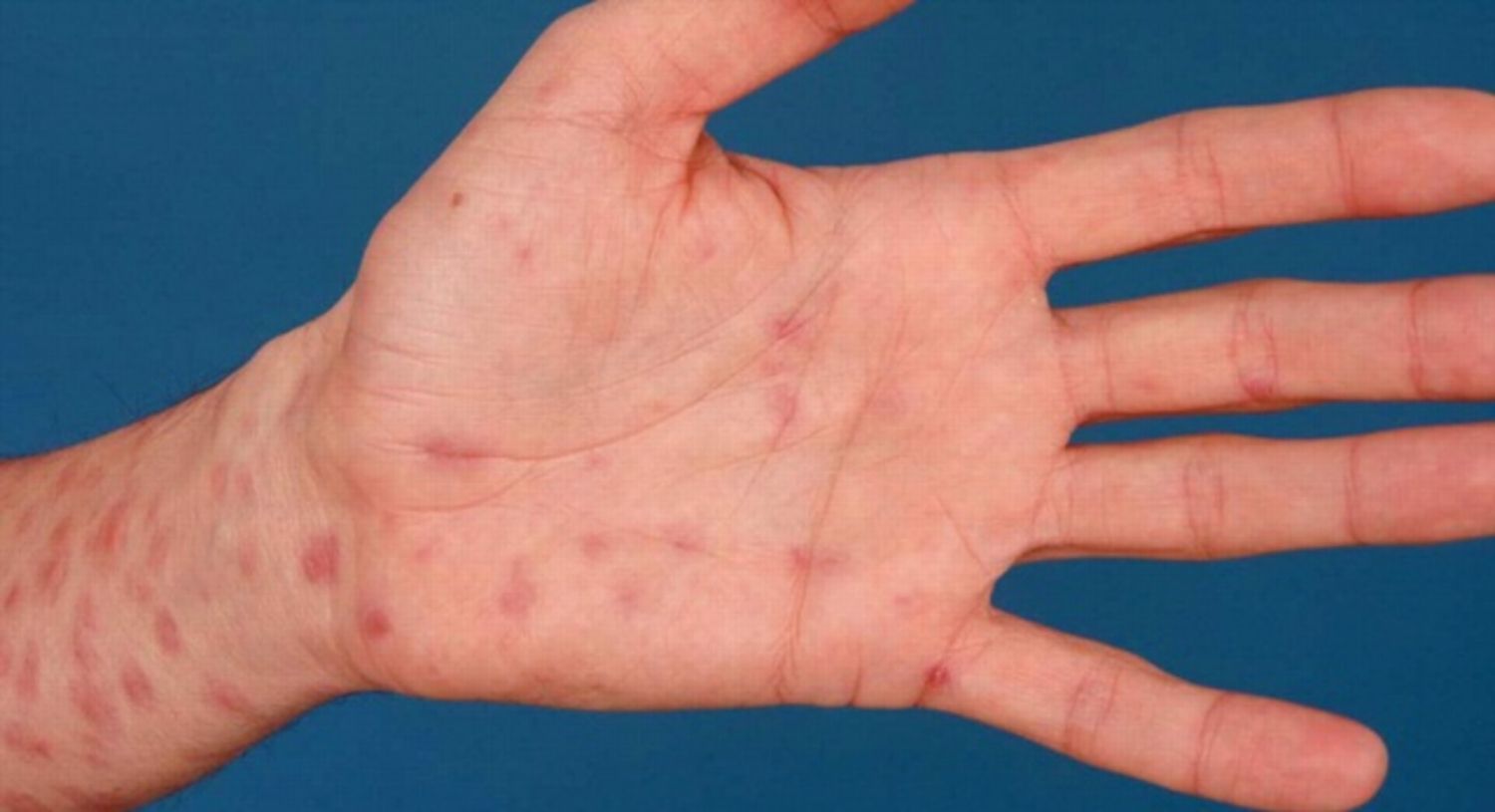
Nếu không được điều trị, thì bệnh giang mai sẽ tiến triển từ giai đoạn đầu sang giai đoạn 2, đó là giang mai thứ phát.
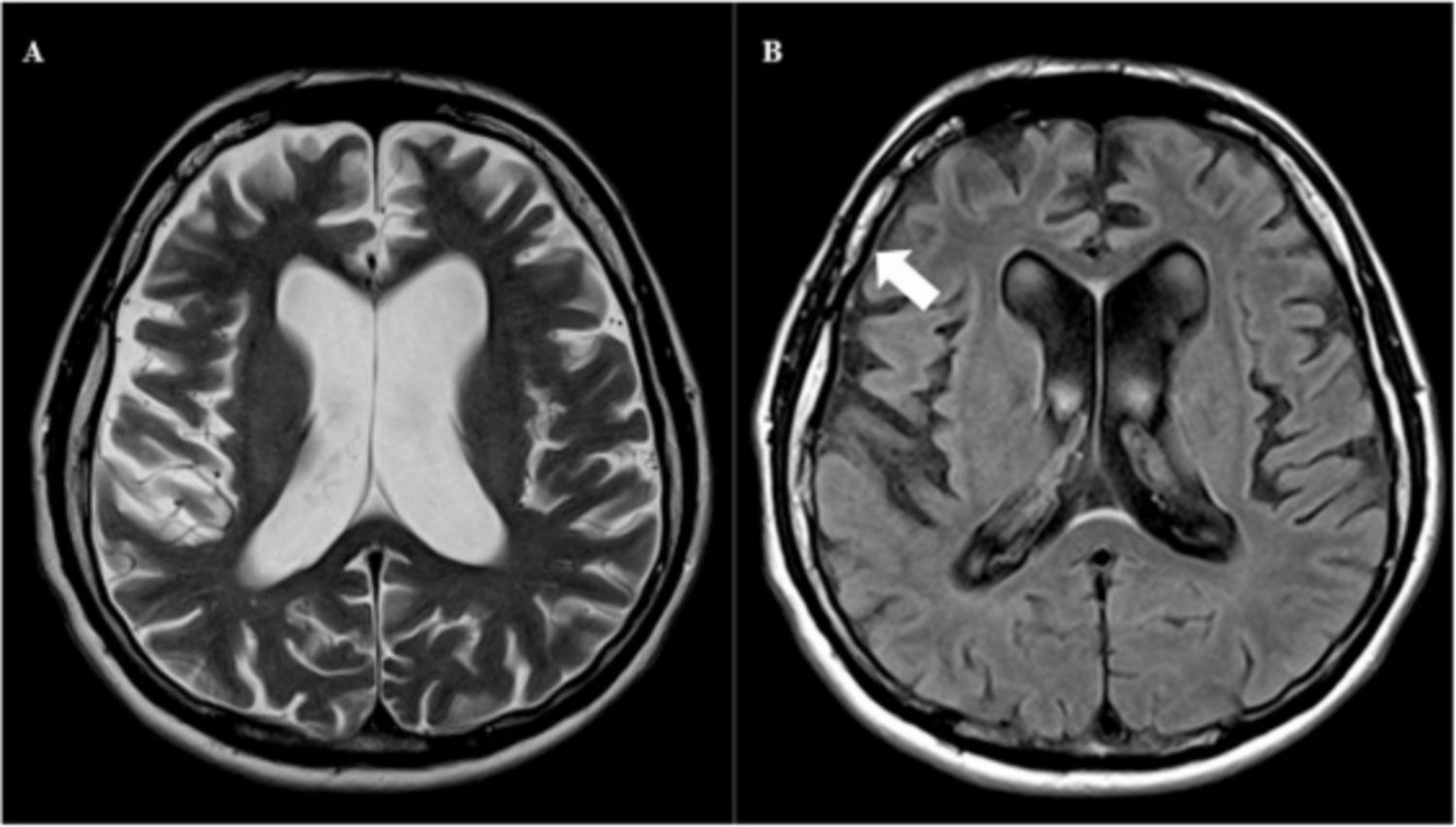
Giang mai thần kinh là một trong các biến chứng của bệnh giang mai.
Viêm màng não do giang mai có thể đe dọa đến tính mạng nếu không được can thiệp kịp thời nhưng hoàn toàn có thể phòng ngừa được.

Câu hỏi: - Bác sĩ có thể cho tôi biết vận động viên nên tuân thủ những hướng dẫn tập luyện nào trong thai kỳ không ạ? Cảm ơn bác sĩ!

Viên đặt phụ khoa sẽ cho hiệu quả điều trị bệnh phụ khoa nhanh hơn so với các loại thuốc đường uống.
- 1 trả lời
- 664 lượt xem
Em sinh thường và đang nuôi con bằng sữa mẹ. Bé được hơn 1 tháng rồi mà vết khâu tầng sinh môn của em vẫn bị đỏ ngứa, viêm nhiễm rất khó chịu. Đi khám, bs cho uống kháng sinh Amoxycilin 500mg. Nhưng em cũng ngại dùng vì sợ thuốc này bài tiết vào sữa, ảnh hưởng đến em bé?
- 1 trả lời
- 558 lượt xem
Bị giang mai giai đoạn 2 kín, em đã chữa được 1 năm và kết quả đang là 1/500 ạ. Giờ, em có thể mang thai lại mà không gây hại gì cho em bé không ạ? Mong bs chỉ giúp xem em phải làm gì để an toàn cho bé ạ?!
- 1 trả lời
- 1553 lượt xem
Vợ chồng em đã có 1 cháu gái 4 tuổi. Hiện vợ em đang sử dụng thuốc ngừa thai, viên màu vàng. Trong quá trình sử dụng, cô ấy chỉ uống đủ những viên màu vàng, còn những viên màu nâu (là thuốc bổ máu) thì lại không chịu uống. Bây giờ, thấy trễ kinh 1 tuần, cô ấy mua que về thử, không thấy lên 2 vạch - Vậy, liệu bà xã em có sao làm không ạ?
- 1 trả lời
- 779 lượt xem
Đi khám, bs cho em hai loại thuốc là saferon 60 viên và calciD 60viên uống vào buổi sáng và trưa. Vậy, em có thể uống 2 viên Saferon buổi sáng còn 2 viên calciD buổi trưa, được không ạ?
- 0 trả lời
- 1905 lượt xem
Trước lúc mang thai 2 tháng em có uống viên này. Mỗi ngày 1 viên. Không biết có ảnh hưởng tới thai không hả bác sĩ? Em cảm ơn