Phần 2: Phương pháp tiếp cận dựa trên Peptide ruột


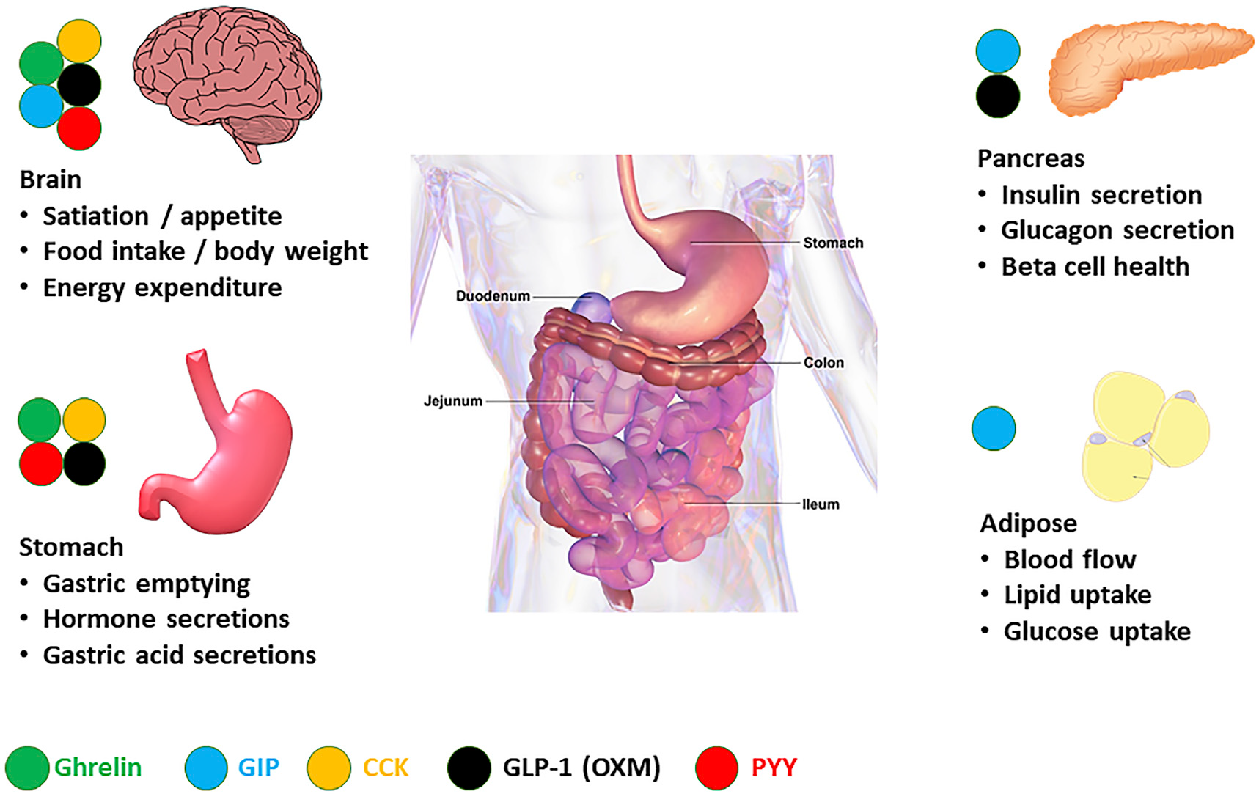
Ở đây, chúng tôi nhấn mạnh một số peptide chính của ruột về vị trí bài tiết, vị trí và cơ quan tác động và các chức năng, nhấn mạnh vào các phân tử có tiềm năng điều trị đã được khám phá trong các nghiên cứu lâm sàng.
Một số peptide này, đặc biệt là GLP-1, nhưng cũng có loại khác Các peptide liên quan đến glucagon, chẳng hạn như insulinotropic phụ thuộc glucosepolypeptide (GIP) và oxyntomodulin (OXM) cũng như peptide tyrosine tyrosine (PYY), đã trở thành liệu pháp quan trọng cho bệnh béo phì và tiểu đường loại 2. Hiệu quả quan sát nơi họ trong số các trị liệu mới hấp dẫn nhất cách tiếp cận trong các lĩnh vực này. Bằng cách nào những nội tiết tố có nguồn gốc từ ruột hoạt động và làm thế nào chúng có thể hoạt động cùng nhau có khả năng bắt chước những ảnh hưởng của phẫu thuật barective là một lĩnh vực nghiên cứu thú vị có khả năng dẫn đến các liệu pháp bổ sung cho bệnh tiểu đường và béo phì.
T2DM.
Chất đồng vận thụ thể GLP-1
GLP-1 tự thân, khá hữu ích để mô tả đặc điểm sinh lý và dược lý của incretin nhưng không phù hợp để sử dụng điều trị do thời gian bán hủy rất ngắn. Exendin-4, giống với GLP-1 Peptide, được phân lập từ nước bọt của quái vật Gila, ổn định hơn, cho phép phát triển trị liệu và exenatide, một chất tổng hợp phiên bản exendin-4 dùng qua đường tiêm hai lần mỗi ngày, là liệu pháp dựa trên GLP-1 đầu tiên để điều trị T2DM được thương mại hóa. Sau đó, chất chủ vận thụ thể GLP-1 kéo dài thích hợp cho việc dùng một lần mỗi ngày hoặc một lần tiêm hàng tuần, bao gồm cả một phác đồ điều trị bằng exenatide, đã được phê duyệt cho sử dụng lâm sàng.
Một số quy luật quan trọng đã được phát hiện thông qua nghiên cứu lâm sàng các chất chủ vận thụ thể GLP-1. Tất cả các phân tử được phê duyệt cho đến nay cho thấy tác dụng hạ đường huyết mạnh, một phần do chúng tác động trực tiếp lên tế bào beta để kích thích tiết insulin phụ thuộc glucose, nhưng cũng một phần do ức chế bài tiết glucagon và, với một số phân tử có tác dụng trì hoãn việc làm rỗng dạ dày. Những phân tử này gây giảm cân, mà chủ yếu được quy cho tác dụng trực tiếp của GLP-1 đối với sự thèm ăn- của tế bào thần kinh điều tiết ở vùng dưới đồi; tác động trên não cũng như các hiệu ứng qua trung gian cũng có thể đóng góp trong những trường hợp nhất định.
Trong khi các chất chủ vận thụ thể GLP-1 tác dụng ngắn cho thấy sự ức chế đáng kể của việc làm rỗng dạ dày, tác dụng này có thể bị suy giảm trong các phân tử tác dụng dài. Buồn nôn và nôn là tác dụng phụ phổ biến nhất và có thể hạn chế liều và do đó hiệu quả điều trị. Phân tử với tỷ lệ đỉnh-đáy thấp hơn dường như có ít tác dụng phụ GI hơn, và những tác dụng phụ này có thể được quản lý thêm thông qua chậm, tăng dần liều dẫn đến liều cao hơn và tốt hơn hiệu quả. Những hiểu biết này đã dẫn đến sự phát triển của hiện tại tạo ra chất chủ vận thụ thể GLP-1 trong đó các phân tử có tối ưu hóa các đặc tính dược động học được cung cấp thông qua tối ưu hóa chế độ dùng thuốc đạt được mức giảm glucose ấn tượng và giảm cân ở bệnh nhân mắc bệnh T2DM. Giảm cân gây ra bởi các phân tử thậm chí còn rõ rệt hơn ở những người không mắc bệnh tiểu đường, dẫn đến phát triển một số các phân tử này như là liệu pháp béo phì.
Nghiên cứu kết quả tim mạch dài hạn, một yêu cầu cho Các chương trình phát triển T2DM, đã tiết lộ các lợi ích bổ sung của các thuốc chủ vận GLP-1. Phần lớn các chất chủ vận thụ thể GLP-1 cho thấy một lợi ích tim mạch, bằng chứng là giảm tai biến nhồi máu cơ tim, đột quỵ và tử vong do tim mạch. Ngoài ra, giảm albumin niệu và giảm tốc độ lọc cầu thận được quan sát thấy trong một số nghiên cứu, nâng cao khả năng lợi ích thận (Các cơ chế cơ bản những lợi ích này không rõ ràng. Chất chủ vận thụ thể GLP-1 liên tục cho thấy tăng nhịp tim và giảm trong máu áp lực, cũng như những cải thiện nhỏ trong hồ sơ lipid huyết thanh, Đáng chú ý nhất là giảm sự tham gia của triglyceride sau bữa ăn và những cải thiện nhỏ về lipoprotein mật độ thấp (LDL) – và lipoprotein mật độ cao (HDL) -cholesterol, cũng như chống viêm tác dụng, có thể góp phần vào tim mạch quan sát và hồ sơ thận (Nauck et al., 2017). Mối quan tâm ban đầu về các vấn đề an toàn tiềm ẩn với thụ thể GLP-1 chất tương tự, bao gồm ung thư biểu mô tuyến tủy và viêm tụy, đã không biểu hiện là vấn đề quan trọng trong phòng khám (Nauck và cộng sự, 2017). Thật vậy, các chất chủ vận thụ thể GLP-1 hiện nay được thiết lập vững chắc trong mô hình xử lý T2DM và là điều trị ưu tiên cho bệnh nhân bị xơ vữa động mạch bệnh, bệnh nhân sẽ được hưởng lợi từ giảm cân, và cá nhân cần phải đạt được sự kiểm soát glucose tuyệt vời mà không cần nguy cơ hạ đường huyết (Hiệp hội tiểu đường Hoa Kỳ, 2019). Làn sóng đổi mới tiếp theo, hiện đang được tiến hành, nhằm mục đích phát triển các phiên bản sinh khả dụng của thuốc chủ vận thụ thể GLP-1 để mở rộng lợi ích của liệu pháp dựa trên GLP-1 đến các giai đoạn trước của mô hình điều trị bệnh tiểu đường.
Các chất đồng vận thụ thể GIP và tính hai mặt của GIP / GLP-1
Không giống như GLP-1, rất ít nghiên cứu đã được tiến hành để phát triển GIP như một liệu pháp độc lập. Ở những người mắc bệnh T2DM, GIP ít ảnh hưởng đến bài tiết insulin, dẫn đến khái niệm bệnh tiểu đường là tình trạng kháng GIP. Trong khi cơ sở phân tử cho kháng GIP không được hiểu rõ, nó đã được tìm thấy liên kết chặt chẽ với tăng đường huyết và khả năng GIP gây ra bài tiết insulin ít nhất có thể được phục hồi một phần bằng phương pháp điều trị bình thường hóa mức glucose bằng insulin hoặc sulfonylureas. Do đó, sự kết hợp của GIP với các chất khác làm giảm glucose có thể giúp giải phóng lợi ích điều trị của nó. Các nghiên cứu về truyền GIP đã thông báo cho sự hiểu biết của chúng tôi về sinh lý và dược lý của GIP. Nổi bật nhất, GIP được biết có tác dụng tăng mức glucagon lưu hành trong điều kiện hạ đường huyết, có khả năng phản ánh tác dụng trực tiếp của GIP trên tế bào alpha tuyến tụy. GIP kích hoạt lưu lượng máu mô mỡ và tăng hấp thu glucose và axit béo vào mô mỡ ở người với mức độ biểu hiện thụ thể GIP cao trong mô mỡ. Không giống như GLP-1, GIP không không ảnh hưởng đến việc làm rỗng dạ dày và không ức chế lượng thức ăn đã được báo cáo với các phân tử GIP được quản lý ngoại vi hoặc tiền lâm sàng hoặc ở người đàn ông.
Khả năng của GIP để kích thích sự hấp thu axit béo vào mỡ mô, cùng với việc quan sát giảm cân ở chuột loại bỏ thụ thể GIP hoặc GIP, đã dẫn đến quan niệm rằng GIP có thể là một phân tử gây béo phì, thúc đẩy sự phát triển chất đối kháng của thụ thể GIP như một phương pháp điều trị bệnh béo phì. Thật thế, kháng thể đối kháng thụ thể GIP hoặc GIP mạnh và chọn lọc giảm trọng lượng cơ thể ở chuột và họ linh trưởng không phải người. Tuy nhiên, các peptide chủ vận GIP tác dụng kéo dài không gây tăng cân ở mô hình tiền lâm sàng, và giảm cân khá mạnh mẽ gây ra bởi GLP-1, thách thức giả định GIP là yếu tố gây béo phì.
Quan sát tác dụng hiệp đồng giảm cân của GIP kết hợp điều trị với GLP-1 trong các mô hình tiền lâm sàng đã thúc đẩy sự phát triển của chất chủ vận thụ thể GIP và GLP-1 kép (cũng được gọi là ‘Twincretins Điện thoại) để điều trị T2DM và béo phì. Đầu tiên các phân tử được thử nghiệm ở người cho thấy glucose đáng kể giảm và giảm cân so với giả dược nhưng không phân biệt bản thân đáng kể từ thụ thể GLP-1 duy nhất chất chủ vận liraglutide trong các nghiên cứu lâm sàng sớm. Gần đây, một chất mới chủ vận thụ thể GIP và GLP-1, (hiện được gọi là tirzepatide), đã cải thiện sâu sắc trong kiểm soát glucose và trọng lượng cơ thể trong một nghiên cứu pha 2b khi so sánh với dulaglutide, một chất chủ vận thụ thể GLP-1. Tirzepatide giảm tới > 15% cân ở khoảng 1/4 bệnh nhân, và làm bình thường hóa đường huyết (HbA1c dưới 5,7%) trong khoảng một phần ba số bệnh nhân, xác định một mức độ hiệu quả mới cho T2DM trị liệu. Các cơ chế sâu xa hiệu quả của tirzepatide còn chưa được hiểu đầy đủ. So với các chất chủ vận thụ thể GIP / GLP-1 kép trước đây, tirzepatide có tiềm năng lớn hơn đối với thụ thể GIP so với thụ thể GLP-1, cung cấp một lời giải thích có thể cho lâm sàng lợi ích sâu sắc của nó. Dữ liệu tiền lâm sàng chứng minh rằng cả thụ thể GIP và GLP-1 góp phần vào hiệu quả hạ đường huyết của tirzepatide. Nghiên cứu lâm sàng đang diễn ra để kiểm tra các cơ chế làm giảm trọng lượng cơ thể- và tác dụng hạ đường huyết của tirzepatide chi tiết hơn. Sẽ khá thú vị để xem liệu các tác dụng đặc trưng của GIP có ảnh hưởng đến lưu lượng máu mô mỡ và sự hấp thu chất dinh dưỡng hay không, có đóng góp vào hiệu quả lâm sàng của tirzepatide và cách vai trò gần đây của GIP trong việc điều chỉnh sự thèm ăn mạch ở chuột có thể điều biến trọng lượng cơ thể trong bối cảnh hành động GLP-1 hay không. Nhìn chung, tirzepatide chứng tỏ tiềm năng của liệu pháp incretin kép và chắc chắn để châm ngòi cho các nghiên cứu bổ sung về các tác dụng của GIP. Tirzepatide Gần đây đã tiến vào thử nghiệm lâm sàng giai đoạn 3 cho T2DM với kế hoạch bổ sung để kiểm tra tác dụng chống béo phì và viêm gan nhiễm mỡ không do rượu (NASH).
OXM -Oxyntomodulin

Chất chủ vận Glucagon và chủ vân kép Glucagon -GLP-1 Receptor ban đầu được mô tả là một trong một số peptide có nguồn gốc từ ruột, Các peptide đáp ứng glucagon gọi chung là ‘glucagon ruột là một sản phẩm axit amin 37 tự nhiên của gen glucagon được tiết ra bởi các tế bào L enteroendocrine trong đáp ứng với bữa ăn, với nồng độ <2 pM và 10 pM trong huyết thanh ăn chay so với trạng thái sau ăn ở người. Phù hợp với một tiền thân chung và bài tiết từ cùng loại tế bào, nồng độ OXM trong huyết thanh tương quan chặt chẽ với mức độ lưu hành GLP-1. Mặc dù không xác định được thụ thể OXM nội sinh, OXM là chất chủ vận yếu cho cả thụ thể glucagon và GLP-1 với tiềm năng thấp hơn từ 10 đến 20 lần so với glucagon hoặc GLP-1. Do nồng độ huyết thanh thấp, OXM không có khả năng đóng góp đáng kể đến tín hiệu thụ thể GLP-1 hoặc glucagon dưới điều kiện bình thường, và chức năng sinh lý của nó vẫn chưa được biết. Thật thú vị, tuy nhiên, sau khi phẫu thuật giảm cân, mức OXM được tăng lên tới 200 pM sau bữa ăn, đạt đến mức có thể được dự kiến sẽ góp phần thay đổi trao đổi chất trong trạng thái này.
Glucagon được biết đến như một loại hormone được tiết ra bởi các tế bào alpha của tuyến tụy tác động lên gan để tăng sản lượng glucose của gan, do đó làm tăng nồng độ glucose máu trong điều kiện hạ đường huyết. Nồng độ glucagon thấp cũng có thể được tiết ra từ ruột, như đã được chứng minh gần đây ở những người bị bệnh tụy, mặc dù ý nghĩa của việc này không rõ ràng. Thật thú vị, glucagon cũng đã được công nhận là một hormone điều tiết trọng lượng. Sử dụng glucagon ức chế ngay lập tức lượng thức ăn và tăng sử dụng năng lượng ở người. Sử dụng hoạt chất tương tự glucagon tác dụng kéo dài làm giảm trọng lượng cơ thể chủ yếu bằng cách tăng tiêu thụ năng lượng, một hiệu ứng có vẻ như trung gian bởi gan thông qua cả FGF21 và FXR. Ở người, glucagon làm tăng nồng độ FGF21 huyết thanh và gây ra phân hủy lipid, cho thấy rằng một số con đường tương tự có thể xảy ra. Mặc dù hiệu quả đầy hứa hẹn của glucagon về điều chỉnh trọng lượng cơ thể, tác dụng phụ gây tăng đường huyết mạnh ở động vật gặm nhấm và con người đã ngăn chặn sự phát triển liệu pháp sử dujgn chất giống với glucagon cho bệnh béo phì hoặc T2DM.
Điều thú vị là sử dụng đồng thời glucagon và GLP-1 trong nghiên cứu tiền lâm sàng lại dẫn đến giảm cân vượt quá những gì có thể đạt được bằng một mình GLP-1 trong khi duy trì tác dụng giảm glucose của GLP-1. Ở người, tác dụng tương tự có thể đạt được bằng dùng OXM ở liều dự kiến sẽ kích hoạt cả glucagon và thụ thể GLP-1. Ở cả hai loại nghiên cứu tiền lâm sàng và ở trên người, glucagon làm tăng tiêu thụ năng lượng, mặc dù còn khiêm tốn, ngay cả khi có mặt của GLP-1. Hơn nữa, trong các mô hình tiền lâm sàng, chuyển hóa lipid đã được cải thiện sâu sắc so với việc sử dụng chất chủ vận thụ thể GLP-1 chọn lọc, cho thấy một lợi ích tiềm tàng trong điều trị của NASH. Những phát hiện này đã gây ra sự quan tâm đáng kể trong việc khám phá sự kết hợp một chất mẹ của glucagon và GLP-1 mà một số các phân tử đang tiến tới thử nghiệm lâm sàng. Các phân tử có tác dụng nhất là SAR425899 và MEDI0382 (hiện được gọi là cotadutide), cho thấy khả năng giảm cân ấn tượng trong nghiên cứu ngắn hạn ở những người bị béo phì hoặc T2DM cũng như làm giảm mỡ ở gan. Tác dụng hạ Glucose máu tương tự như những gì sẽ được quan sát thấy ở các chất chủ vận thụ thể GLP-1, gợi ý rằng các phân tử này có thể cân bằng hoạt động GLP-1 và glucagon. Điều quan trọng cần lưu ý là cho đến nay chưa có so sánh trực tiếp của glucagon / Chất chủ vận kép thụ thể GLP-1/Glucagon với chất chủ vận thụ thể GLP-1 đơn ở người. Trong khi MEDI0382 đã được đưa vào các nghiên cứu pha 2b cho T2DM, béo phì và NASH, SAR425899, cũng chất chủ vận kép của thụ thể glucagon / GLP-1 khác, MRK-8521, đã bị ngưng sử dụng, có khả năng phản ánh những thách thức trong việc phát triển chất chủ vận thụ thể glucagon / GLP-1 đa chức năng.
Đồng thời với sự phát triển của các chất chủ vận kép tương tự, những nỗ lực đang tiến hành là kết hợp các đặc điểm dược lý của GLP-1, GIP và glucagon để giảm cân thậm chí nhiều hơn. Trong các mô hình tiền lâm sàng, những kết hợp này có thể đưa trọng lượng cơ thể của chuột rất béo phì về bình thường và hiệu quả tương tự có thể đạt được với phân tử chức năng kép. Các bộ ba tam giác GLP-1, GIP và glucagon. Một số bộ ba phân tử không phân tử hiện đang được phát triển, với ít nhất ba phân tử trong lâm sàng sớm thử nghiệm (PYY) Một peptide có nguồn gốc từ ruột có thể đóng vai trò bổ sung cho GLP-1 là PYY.
PYY
PYY là một peptide 36 axit amin thuộc họ polypeptide tụy (PP), bao gồm PP được tiết ra từ tuyến tụy và neuropeptide Y (NPY) được sản xuất bởi các tế bào thần kinh trong CNS. Trong khi bao gồm các kẹp tóc tương tự cấu trúc mô-đun và chia sẻ cùng NPY kết hợp G-protein. Các thụ thể (Y1, Y2, Y4 và Y5), PYY chủ yếu được tiết ra từ các tế bào L của ruột và khác biệt về chức năng với PP và NPY.
PYY tồn tại ở hai dạng nội sinh, PYY1-36 và PYY3-36, sự khác biệt về sự phong phú trong việc nhịn ăn so với các trạng thái sau bữa ăn và trong sự chọn lọc đối với các thụ thể NPY. Tương tự như GLP-1, Nồng độ PYY tăng sau bữa ăn và tương quan với việc kéo dài giảm cân có được sau 8 tuần ăn kiêng ít calo duy trì giảm cân trong 1 năm. PYY3- 36 được sản xuất từ PYY1-36 thông qua hoạt động của dipeptidyl peptidase IV (DPP4) và là hình thái lưu thông chính sau ăn của PYY. Không giống như GLP-1, sự phân cắt enzyme của PYY1-36 của DPP4 không làm giảm ái lực của PYY xuống một thụ thể; thay vào đó, nó cải thiện tính chọn lọc. Do đó, trong khi PYY1-36 liên kết tất cả các thụ thể NPY, PYY3-36 hoạt động như một chất chủ vận Y2 chọn lọc, do đó nó thể hiện hành động độc đáo của nó.
Được phát hiện vào đầu những năm 1980, các báo cáo đầu tiên cho thấy một vai trò hạn chế của PYY trong đường tiêu hóa, bao gồm cả việc thúc đẩy bài tiết dạ dày, tuyến tụy và kiểm soát nhu động ruột. Tuy nhiên, người ta phát hiện ra rằng PYY3-36 đóng vai trò trong cân bằng năng lượng nội môi thông qua tác động trung ương được chứng minh bằng các thí nghiệm nơi sử dụng PYY3-36 ngoại sinh làm ăn giảm thức ăn ở cả loài gặm nhấm và người và làm giảm trọng lượng cơ thể đạt được trong các loài gặm nhấm, thông qua thụ thể Y2 như một mục tiêu tiềm năng trong điều trị bệnh chuyển hóa. Hơn nữa, có bằng chứng cho thấy PYY có thể đóng một vai trò trong nhạy cảm với insulin và sự hấp thu glucose, có khả năng thông qua thụ thể Y2. Trong khi những cơ chế vẫn đang được nghiên cứu mạnh mẽ, lợi ích của tác động nhạy cảm với insulin để điều trị các bệnh chuyển hóa không nên làm quá lên.
PYY và GLP-1 đã được chứng minh là cùng ở trong tế bào L cùng tiết ra từ 1 túi tiết và xuất hiện để đáp ứng với các kích thích tương tự, gợi ý rằng PYY và GLP-1 đóng vai trò bổ trợ nhau. Thêm nữa, truyền cùng lúc PYY3-36 và GLP-1 tạo ra tác đụng hiệp đồng làm giảm ăn ở người và các nghiên cứu về độc tính cấp tính và mãn tính ở loài gặm nhấm chứng minh tác dụng phụ gia và / hoặc hiệp đồng của PYY3-36 và GLP-1 về những cải tiến trong cân bằng năng lượng nội môi. Trong khi tác dụng phụ trên đường tiêu hóa có thể hạn chế sử dụng các chất tương tự PYY3-36 chủ vận thụ thể Y2 như một mục tiêu điều trị, đặc biệt là khi kết hợp một chất tương tự GLP-1 với chất tương tự PYY tác dụng kéo dài làm giảm được lượng thức ăn ở loài linh trưởng không phải người với sự mô phỏng tối thiểu, thậm chí khi phối hợp thêm với liraglutide làm giảm thêm thức ăn lượng ăn vào. Một số chất tương tự PYY3-36 tác dụng dài hạn và chất chủ vận thụ thể Y2 đang được thử nghiệm lâm sàng sớm phát triển và dự đoán rằng các phân tử này cuối cùng sẽ được thử nghiệm kết hợp với các chất tương tự GLP-1. Ngoài ra, các cách tiếp cận đồng phân tử đối với PYY / GLP1 đang được nghiên cứu tiền lâm sàng.

Tập thể dục là “liều thuốc tốt” để kiểm soát huyết áp, nếu tập thể dục thường xuyên huyết áp sẽ dần trở về bình thường và giúp cơ thể khỏe mạnh. Tập gym là hình thức tập thể dục, vậy người bị cao huyết áp có nên tập gym?
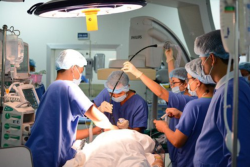
Rung nhĩ là rối loạn nhịp tim thường gặp nhất hiện nay và có tỷ lệ mắc tăng dần theo tuổi. Khoảng 4% trường hợp rung nhĩ xảy ra ở các bệnh nhân tuổi 8% bệnh nhân độ tuổi 80 trở lên có rung nhĩ.
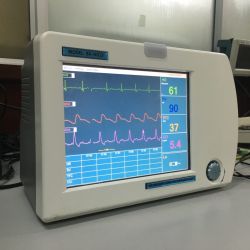
Đặt stent trong nhồi máu cơ tim là thủ thuật ngoại khoa được áp dụng trong điều trị tim mạch. Đặt stent được chỉ định với trường hợp nhồi máu cơ tim cấp, mạch vành bị tắc hẹp nặng không đáp ứng tốt với điều trị của thuốc.

Nhồi máu cơ tim hay bệnh động mạch vành cấp tính là một bệnh lý nguy hiểm thường gặp ở người cao tuổi. Tỷ lệ tử vong do các bệnh lý tim mạch vẫn còn cao dù đã có xu hướng giảm so với trước đây. Hiện nay có 5 type nhồi máu cơ tim khác nhau và hay gặp nhất là nhồi máu cơ tim type 1.
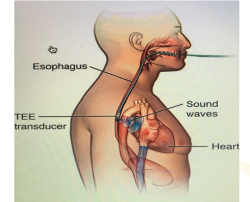
Siêu âm tim là phương pháp chẩn đoán hình ảnh không xâm lấn, an toàn và được sử dụng rất phổ biến trong xác định những bất thường của tim.

Các loại thực phẩm chúng ta ăn hàng ngày có hàng chục loại chất béo khác nhau, và mỗi loại lại có một vai trò và tác động không giống nhau bên trong cơ thể.