Helicobacter pylori Real-time PCR - Bộ y tế 2018
I. MỤC ĐÍCH VÀ NGUYÊN LÝ
1. Mục đích
- Phát hiện DNA đ c trưng c a Helicobacter pylori từ mảnh sinh thiết dạ dày.
2. Nguyên lý
- Dựa trên nguyên lý c a kỹ thuật Real-time PCR.
II. CHUẨN BỊ
1. Người thực hiện
- Người thực hiện: Nhân viên xét nghiệm đã được đào tạo và có chứng chỉ ho c chứng nhận v chuyên ngành Vi sinh (và/ho c sinh học phân tử/ sinh học/công nghệ sinh học).
- Người nhận định và phê duyệt kết quả: Người thực hiện có trình độ đại học ho c sau đại học v chuyên ngành Vi sinh (và/ho c sinh học phân tử/ sinh học/công nghệ sinh học).
2. Phương tiện, hóa chất (Ví dụ hoặc tương đương)
2.1. Trang thiết bị
- Máy real-time PCR và hệ thống máy vi tính
- Bộ lưu điện
- T an toàn sinh học cấp 2
- Máy ly tâm dùng cho tube 0,2ml
- Máy ly tâm > 12000 gpm/phút
- Máy nhiệt
- Máy vortex
- Chày cối nghi n
- T lạnh 2oC - 8 oC
- T âm sâu (-20oC) ho c (-70oC)
- Micropipettes các thể tích từ 5-1000μl
2.2. Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)

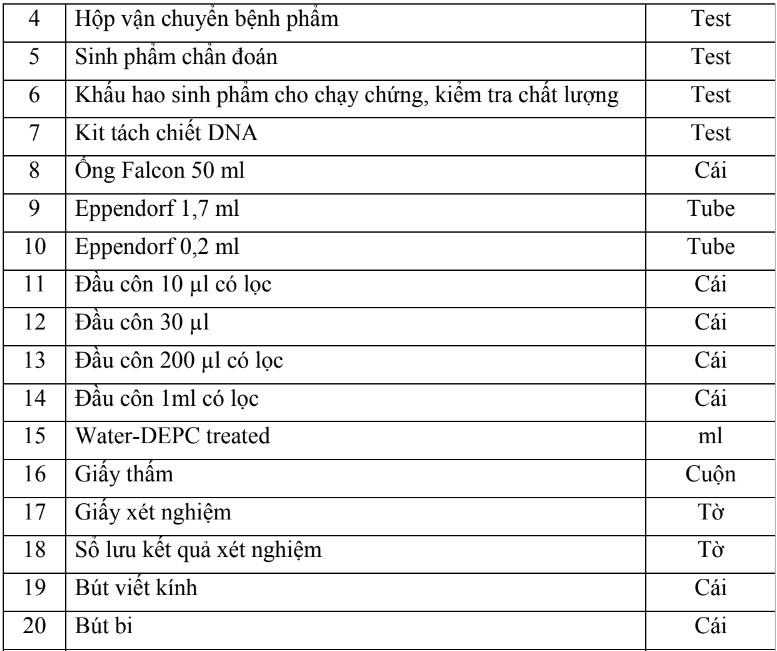
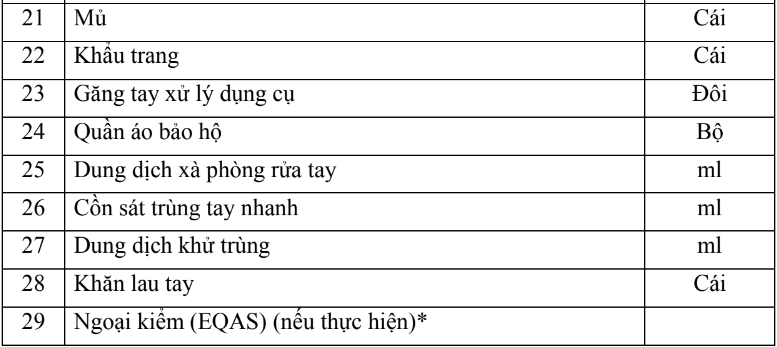
* Ghi chú:
- Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/50 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 3 lần/1 năm).
3. Bệnh phẩm
- Mảnh sinh thiết dạ dày.
4. Phiếu xét nghiệm
- Đi n đầy đ thông tin theo mẫu yêu cầu
III. CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ trên.
1. Lấy bệnh phẩm
- Lấy qua ống nội soi đường miệng
- Quan sát thấy ổ loét, lấy 4 mẫu (3 mẫu các góc tổn thương loét, lấy vùng mép (ranh giới) c a tổn thương và một mảnh trung tâm) ho c lấy các vị trí có tổn thương nghi ngờ do H. pylori (trợt, niêm mạc sần,...)
- Dùng kim lấy máu chuyển bệnh phẩm từ kim sinh thiết vào lọ đựng bệnh phẩm.
2. Tiến hành kỹ thuật:
Bộ sinh phẩm H. pylori Real-TM (Sacace –VD ho c tương đương)
- Thu nhận và xử lý mẫu
- Tách chiết DNA
- Thực hiện phản ứng real-time PCR
IV. NHẬN ĐỊNH KẾT QUẢ
1. Điều kiện của phản ứng
- Chứng dương có đường biểu diễn tín hiệu huỳnh quang màu JOE dương tính và đường biểu diễn tín hiệu huỳnh quang màu FAM âm tính.
- Chứng âm có đường biểu diễn tín hiệu huỳnh quang màu FAM dương tính, đường biểu diễn tín hiệu huỳnh quang màu JOE âm tính.
2. Phân tích mẫu
- Mẫu dương tính: Mẫu có đường biểu diễn dương tính rõ ràng với màu bắt đầu từ chu kỳ 36 tr v trước.
- Mẫu nghi ngờ: Mẫu có đường biểu diễn dương tính và bắt đầu từ sau chu kỳ 36 đ nghị lấy mẫu lại để thực hiện xét nghiệm.
- Mẫu âm tính: Mẫu có đường biểu diễn âm tính, chứng nội phải dương tính.
3. In đồ thị kết quả
V. NHỮNG SAI SÓT CẦN XỬ TRÍ
- Nếu đường đồ thị huỳnh quang c a mẫu xuất hiện ngoài chu kỳ thứ 40 thì phải cẩn thận kiểm tra và đánh giá lại mẫu.
Hướng dẫn quy trình kỹ thuật chuyên ngành Vi sinh - Bộ y tế 2018
Hướng dẫn quy trình kỹ thuật chuyên ngành Vi sinh - Bộ y tế 2018
Hướng dẫn quy trình kỹ thuật chuyên ngành Vi sinh - Bộ y tế 2018
Hướng dẫn quy trình kỹ thuật chuyên ngành Vi sinh - Bộ y tế 2018
Hướng dẫn chẩn đoán và điều trị một số bệnh thường gặp ở trẻ em - Bộ y tế 2015